
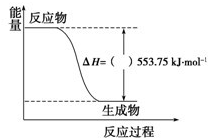
 (1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:
(1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:| 镁/800C/Ar |
| ||
| ||
| ||


科目:高中化学 来源: 题型:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/100kPa | 4.56 | 5.14 | 5.87 | 6.30 | 7.24 | 8.16 | 8.18 | 8.20 | 8.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(CH3)2CHCH2Br在碱性溶液中水解 |
| B、苯在催化剂FeCl3作用下与Cl2反应 |
C、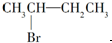 与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 |
D、 在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、既能与有机物反应又能与无机物反应 |
| B、既能发生复分解反应又能发生水解反应 |
| C、既能发生置换反应又能发生酯化反应 |
| D、既能发生取代反应又能发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
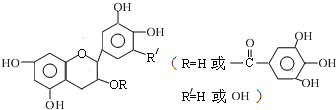
| A、常温下,儿茶素不溶于水,也不溶于有机溶剂 |
| B、儿茶素能与FeCl3溶液发生显色反应 |
| C、1mol儿茶素最多可与9mol NaOH反应 |
| D、儿茶素一定不能发生水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com