
【题目】三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废水(镍主要以NiR2络合物形式存在)制取草酸镍(NiC2O4),再高温灼烧草酸镍制取三氧化二镍。工艺流程如图所示:
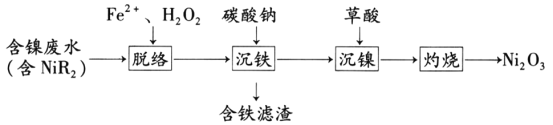
已知:①NiR2(aq)![]() Ni2+(aq)+2R-(aq)(R-为有机物配体,K=1.6×10-14)
Ni2+(aq)+2R-(aq)(R-为有机物配体,K=1.6×10-14)
②Ksp[Fe(OH)3]=2.16×10-39,Ksp[Ni(OH)2]=2×10-15
③Ka1(H2C2O4)= 5.6×10-2,Ka2(H2C2O4)= 5.4×10-5
④“脱络”过程中,R-与中间产物·OH反应生成·R(有机物自由基),·OH能与H2O2发生反应。有关反应的方程式如下:
i.Fe2++H2O2=Fe3++OH-+·OH
ii.R-+·OH = OH-+·R
iii.H2O2+2·OH=O2↑+2H2O
请回答下列问题:
(1)中间产物·OH的电子式是________
(2)“沉铁”时,若溶液中c(Ni2+)=0.01mol·L-1,加入碳酸钠调溶液的pH为________(假设溶液体积不变,lg6≈0.8)使Fe3+恰好沉淀完全(离子的浓度≤1.0×10-5mol·L-1),此时________(填“有”或“无”)Ni(OH)2沉淀生成。
(3)25℃时,pH=3的草酸溶液中c(C2O42-)/c(H2C2O4)________(保留两位有效数字)。“沉镍”即得到草酸镍沉淀,其离子方程式是________
(4)“灼烧”氧化草酸镍的化学方程式为_______________________________。
(5)加入Fe2+和H2O2能够实现“脱络”的原因是________。
(6)三氧化二镍能与浓盐酸反应生成氯气,写出反应的离子方程式________________。
【答案】![]() 2.8 无 3.02 Ni2+ +H2C2O4 = NiC2O4↓ + 2H+ 4NiC2O4 +3O2
2.8 无 3.02 Ni2+ +H2C2O4 = NiC2O4↓ + 2H+ 4NiC2O4 +3O2![]() 2Ni2O3 +8CO2↑ Fe2+和H2O2发生反应生成·OH,·OH将R-转化成·R,c(R-)减小,使平衡NiR2(aq)
2Ni2O3 +8CO2↑ Fe2+和H2O2发生反应生成·OH,·OH将R-转化成·R,c(R-)减小,使平衡NiR2(aq)![]() Ni2+(aq)+2R-(aq)向正向移动,实现“脱络” Ni2O3 +6H+ +2Cl- = 2Ni2+ +Cl2↑ +3H2O
Ni2+(aq)+2R-(aq)向正向移动,实现“脱络” Ni2O3 +6H+ +2Cl- = 2Ni2+ +Cl2↑ +3H2O
【解析】
(1)·OH有一个孤电子,据此书写其电子式;
(2)根据氢氧化铁的溶度积,计算要使Fe3+恰好沉淀完全所需的c(OH),进而计算得出其pH值,再根据Ni2+与溶液中c(OH)的平方的乘积与Ksp[Ni(OH)2]比较,得出溶液中是否有沉淀生成;
(3)依据二元弱酸草酸的两步电离平衡常数表达式方程式列式计算;流程中加入草酸后变为草酸镍,据此作答;
(4)“灼烧”过程产生了Ni2O3,依据氧化还原反应规律书写化学方程式;
(5)依据给定条件④,Fe2+和H2O2发生反应生成·OH,·OH将R-转化成·R,c(R-)减小,考虑平衡NiR2(aq)![]() Ni2+(aq)+2R-(aq)移动情况分析作答;
Ni2+(aq)+2R-(aq)移动情况分析作答;
(6)根据得失电子数守恒书写其化学方程式。
(1)·OH有一个孤电子,核外为9个电子,其电子式为:![]() ;
;
(2)Ksp[Fe(OH)3]=2.16×10-39,则使Fe3+恰好沉淀完全所需的c(OH) = ![]() = 6 ×10-12,此时溶液的pH = -lgc(H+) = -lg
= 6 ×10-12,此时溶液的pH = -lgc(H+) = -lg![]() = 2 +lg6 = 2.8,因溶液中c(Ni2+)=0.01mol·L-1,则c(Ni2+)×c2(OH) = 0.01mol·L-1×(6×10-12)2 = 3.6×10-25 < Ksp[Ni(OH)2],因此无Ni(OH)2沉淀,
= 2 +lg6 = 2.8,因溶液中c(Ni2+)=0.01mol·L-1,则c(Ni2+)×c2(OH) = 0.01mol·L-1×(6×10-12)2 = 3.6×10-25 < Ksp[Ni(OH)2],因此无Ni(OH)2沉淀,
故答案为:2.8;无;
(3)草酸在水溶液中发生电离,第一电离方程式为:H2C2O4![]() H+ + HC2O4-,其电离平衡常数Ka1(H2C2O4) =
H+ + HC2O4-,其电离平衡常数Ka1(H2C2O4) = ![]() ,同理第二步电离方程式为:HC2O4-
,同理第二步电离方程式为:HC2O4-![]() H+ + C2O42-,其电离平衡常数Ka2(H2C2O4) =
H+ + C2O42-,其电离平衡常数Ka2(H2C2O4) = ![]() , c(C2O42-)/c(H2C2O4) =
, c(C2O42-)/c(H2C2O4) = ![]() ×
×![]() ×
× ![]() = Ka2(H2C2O4)× Kal(H2C2O4)×
= Ka2(H2C2O4)× Kal(H2C2O4)× ![]() = 5.4×10-5 × 5.6×10-2 ×
= 5.4×10-5 × 5.6×10-2 ×![]() 3.02,沉镍过程加入草酸,其离子方程式为:Ni2+ +H2C2O4 = NiC2O4↓ + 2H+,
3.02,沉镍过程加入草酸,其离子方程式为:Ni2+ +H2C2O4 = NiC2O4↓ + 2H+,
故答案为:3.02;Ni2+ +H2C2O4 = NiC2O4↓ + 2H+;
(4)“灼烧”氧化草酸镍生成Ni2O3,C元素以稳定的二氧化碳形式生成,O元素化合价降低,其化学方程式可表示为:4NiC2O4 +3O2![]() 2Ni2O3 +8CO2↑,
2Ni2O3 +8CO2↑,
故答案为:4NiC2O4 +3O2![]() 2Ni2O3 +8CO2↑;
2Ni2O3 +8CO2↑;
(5)根据已知信息可知,Fe2+和H2O2会发生反应生成·OH,·OH将R-转化成·R,c(R-)减小,使平衡NiR2(aq)![]() Ni2+(aq)+2R-(aq)向正向移动,实现“脱络”,
Ni2+(aq)+2R-(aq)向正向移动,实现“脱络”,
故答案为:Fe2+和H2O2发生反应生成·OH,·OH将R-转化成·R,c(R-)减小,使平衡NiR2(aq)![]() Ni2+(aq)+2R-(aq)向正向移动,实现“脱络”;
Ni2+(aq)+2R-(aq)向正向移动,实现“脱络”;
(6)三氧化二镍能与浓盐酸反应生成氯气,镍元素以Ni2+形式存在于溶液中,其离子方程式为:Ni2O3 +6H+ +2Cl- = 2Ni2+ +Cl2↑ +3H2O
故答案为:Ni2O3 +6H+ +2Cl- = 2Ni2+ +Cl2↑ +3H2O。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】已知: A是石油裂解气的主要成份且A的产量通常用来衡量一个国家的石油化工水平;D是常用作厨房中调味品。请回答下列问题:
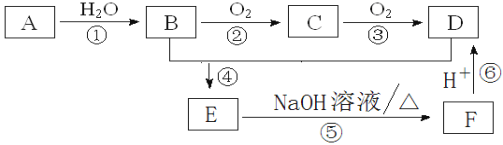
(1)写出C的结构简式________________________。
(2)写出下列反应的反应类型: ①________________,④________________。
(3)写出下列反应的化学方程式:
②______________________________________________________________。
⑤______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华法林(Warfarin)又名杀鼠灵,被美国食品药品监督管理局批准为心血管疾病的临床药物。其合成路线(部分反应条件略去)如下所示:

回答下列问题:
(1)A的名称为_______,E中官能团名称为________。
(2)B的结构简式为________。
(3)由C生成D的化学方程式为_________
(4)⑤的反应类型为______,⑧的反应类型为_________。
(5)F的同分异构体中,同时符合下列条件的同分异构体共有__________种。
a.能与FeCl3溶液发生显色反应 b.能发生银镜反应
其中核磁共振氢谱为五组峰的结构简式为_________。
(6)参照上述合成路线,设计一条由苯酚(![]() )、乙酸酐(CH3CO)2O和苯甲醛(
)、乙酸酐(CH3CO)2O和苯甲醛(![]() )为原料,制备
)为原料,制备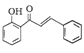 的合成路线(其他无机试剂任选)_____。
的合成路线(其他无机试剂任选)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列8种晶体,用序号回答下列问题:
A.水晶 B.白磷 C.冰醋酸 D.固态氩 E.氯化铵 F.铝 G.金刚石
(1)含有非极性键的原子晶体是_________ ,属于原子晶体的化合物是_______,不含化学键的分子晶体是 _______,属于分子晶体的单质是_________
(2)含有离子键、共价键、配位键的化合物是___________,受热熔化,需克服共价键的是___________.
(3)金刚砂(SiC)的结构与金刚石相似,硬度与金刚石相当,则金刚砂的晶胞中含有_____个硅原子,______个碳原子;金刚石熔点高于金刚砂的原因_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5mol·L—1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有浓度均为0.1 mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水.请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)___________。
(2)④、⑤、⑥、⑦四种溶液中NH![]() 浓度由大到小的顺序是(填序号)_______________。
浓度由大到小的顺序是(填序号)_______________。
(3)将③和④按体积比1∶2混合后,混合液中各离子浓度由大到小的顺序是:__________________。
(4)已知t ℃时,KW=1×10-13,则t ℃(填“>”、“<”或“=”)________25℃。在t ℃时将pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。
I. K2Cr2O7曾用于检测司机是否酒后驾驶:
Cr2O72-(橙色)+CH3CH2OH![]() Cr3+(绿色)+CH3COOH (未配平)
Cr3+(绿色)+CH3COOH (未配平)
(1)基态Cr 原子的价电子轨道表达式为_________________。
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为___________,碳原子的轨道杂化类型为_________,所含σ键与π键的数目之比为______________________。
(3)已知Cr3+等过渡元素水合离子的颜色如下表所示:
离子 | Se3+ | Cr3+ | Fe2+ | Zn2+ |
水合离子的颜色 | 无色 | 绿色 | 浅绿色 | 无色 |
请根据原子结构推测Se3+、Zn2+的水合离子为无色的原因为_______________________。
II. ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。
(4) Fe[Zn(OH)Cl2]2溶液中不存在的微粒间作用力有________(填选项字母);
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
溶液中[Zn(OH)Cl2]-的结构式为_____________________。
III.锌是人体必需的微量元素之一,其堆积方式如图1,晶胞结构如图2。

(5)锌的堆积方式为_________,配位数为__________________。
(6)若梓原子的半径为a pm,阿伏加德罗常数的值为NA,则锌晶体的密度为______g/㎝3 (用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃1体积只能与1体积HBr发生加成反应,生成溴代烷,此溴代烷1mol可与5mol Cl2发生完全取代反应,则该烃的结构简式为( )
A.CH2=CH2B.CH3CH=CH2
C.CH3CH3D.CH2=CH—CH=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积 0.1mol/L 醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH (pOH = -lg[OH-])与pH的变化关系如图所示,则
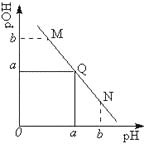
A. M点所示溶液导电能力强于Q点
B. N点所示溶液中c(CH3COO-)﹥c(Na+)
C. M点和N点所示溶液中水的电离程度相同
D. Q点消耗NaOH溶液的体积等于醋酸溶液的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com