
【题目】Ⅰ.CH4和CO2可以制造价值更高的化学产品。已知:
CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH 1=a kJ/mol
CO2(g)+2H2O(g) ΔH 1=a kJ/mol
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH 2=b kJ/mol
CO2(g)+H2(g) ΔH 2=b kJ/mol
2CO(g)+O2(g)![]() 2CO2(g) ΔH 3=c kJ/mol
2CO2(g) ΔH 3=c kJ/mol
(1)求反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH = kJ/mol(用含a、b、c的代数式表示)。
2CO(g)+2H2(g) ΔH = kJ/mol(用含a、b、c的代数式表示)。
(2)一定条件下,等物质的量的(1)中反应生成的气体可合成二甲醚(CH3OCH3),同时还产生了一种可参与大气循环的无机化合物,该反应的化学方程式为 。
(3)用Cu2Al2O4做催化剂,一定条件下发生反应:CO2(g)+CH4(g)![]() CH3COOH(g),温度与催化剂的催化效率和乙酸的生成速率的关系如图,回答下列问题:
CH3COOH(g),温度与催化剂的催化效率和乙酸的生成速率的关系如图,回答下列问题:
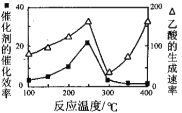
①250~300℃时,乙酸的生成速率降低的原因是 。
②300~400℃时,乙酸的生成速率升高的原因是 。
Ⅱ.钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2Sx )分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
Na2Sx ![]() 2Na+xS (3<x<5)
2Na+xS (3<x<5)
物质 | Na | S | Al2O3 |
熔点/℃ | 97.8 | 115 | 2050 |
沸点/℃ | 892 | 444.6 | 2980 |

(4)根据上表数据,判断该电池工作的适宜温度应为 (填字母序号)。
A.100℃以下
B.100℃~300℃
C.300℃~350℃
D.350℃~2050℃
(5)关于钠硫电池,下列说法正确的是 (填字母序号)。
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为![]() 2e
2e![]() xS
xS
(6)25℃时,若用钠硫电池作为电源电解500mL 0.2mol/L NaCl溶液,当溶液的pH变为13时,电路中通过的电子的物质的量为 mol,两极的反应物的质量差为 g。(假设电解前两极的反应物的质量相等)
【答案】Ⅰ.(1)a +2b –2c
(2)3CO + 3H2 ![]() CH3OCH3 + CO2
CH3OCH3 + CO2
(3)①催化剂的催化效率降低,化学反应速率降低 ②温度升高,化学反应速率加快
Ⅱ.(4)C
(5)AD
(6)0.05 2.3
【解析】本题考查了盖斯定律的应用、氧化还原反应方程式书写、影响反应速率的因素、原电池和电解池。
Ⅰ.(1)已知①CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) △H1=a kJ/mol
CO2(g)+2H2O(g) △H1=a kJ/mol
②CO(g)+H2O(g)![]() CO2(g)+H2(g) △H2=b kJ/mol
CO2(g)+H2(g) △H2=b kJ/mol
③2CO(g)+O2(g)![]() 2CO2(g) △H3=c kJ/mol
2CO2(g) △H3=c kJ/mol
据盖斯定律,①+2×②2×③得:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H=(a+2b2c)kJ/mol;
2CO(g)+2H2(g) △H=(a+2b2c)kJ/mol;
(2)根据反应物和生成物可知,参与大气循环的无机化合物为二氧化碳,据原子守恒书写化学方程式为:3CO+3H2![]() CH3OCH3+CO2;
CH3OCH3+CO2;
(3)①温度超过250℃时,催化剂的催化效率降低,所以温度升高而乙酸的生成速率降低;
②温度升高,化学反应速率加快,故答案为:温度升高,化学反应速率加快;
Ⅱ.(4)原电池工作时,控制的温度应为满足Na、S为熔融状态,则温度应高于115℃而低于444.6℃,只有C符合;
(5)A.通过以上分析知,充电时A是阴极,应该连接电源负极,正确;B.放电时,B是正极、A是负极,Na+由A向B移动,错误;C.充电时,电极A发生还原反应,应连接电源的负极,错误;D.充电时,B是阳极,电极反应式为![]() 2e
2e![]() xS,正确;故答案为:AD;
xS,正确;故答案为:AD;
(6)电解NaCl溶液的反应式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,每生成2 mol NaOH转移电子2 mol,当溶液的pH变为13时,c(OH)=0.1 mol/L,生成NaOH物质的量为0.05 mol,转移电子0.05 mol;转移0.05 mol电子,负极Na质量减少1.15 g,正极质量变化1.15 g,两极的反应物的质量差为2.3 g。
2NaOH+H2↑+Cl2↑,每生成2 mol NaOH转移电子2 mol,当溶液的pH变为13时,c(OH)=0.1 mol/L,生成NaOH物质的量为0.05 mol,转移电子0.05 mol;转移0.05 mol电子,负极Na质量减少1.15 g,正极质量变化1.15 g,两极的反应物的质量差为2.3 g。


科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A.有机物只能在生物体内才能合成
B.有机物都是难溶于水而易溶于有机溶剂的共价化合物
C.完全燃烧只生成CO2和H2O的有机物一定是烃
D.有机物是含有碳元素的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,我国城市环境污染中的大气污染物主要是 ( )
A.NH3、NO、CO2、雾 B.CO2、N2、Cl2、酸雨
C.SO2、NO2、CO、烟尘 D.HCl、SO2、N2、沙尘暴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(HF)2(g) ![]() 2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是( )
2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是( )

A. 温度:T1< T2
B. 平衡常数:K(a)=K(b)<K(c)
C. 反应速率:v(b)>v(a)
D. 当![]() 30g·mol-1时,n(HF):n[(HF)2]=2:1
30g·mol-1时,n(HF):n[(HF)2]=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有:①6.72L CH4,②3.01×1023个HCl分子,③13.6g H2S,④0. 2molNH3。下列对这四种气体相关量的比较不正确的是
A. 体积:②>③>①>④ B. 密度:②>③>④>①
C. 质量:②>③>①>④ D. 氢原子数:①>④>③>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒸馏是实验室制备蒸馏水的常用方法,如图所示的两个装置都可以制取蒸馏水。

(1)图I是实验室制取蒸馏水的常用装置,仪器A的名称是________________,加热A时要加垫石棉网,目的是_______________。
(2)水的流向是否正确?________(填“正确”或“不正确”)
(3)实验时A中除加入少量自来水外,还需加入少量___________,其作用是____________。
(4)图Ⅱ装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图I完全相同。该装置中使用的玻璃导管较长,其作用是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质分类是化学研究的重要方法之一。化学工作者经常根据物质的组成对物质进行分类研究。近年来发现,在金星大气层中存在三氧化二碳。下列物质与它属于同类的是
A、H2、O3 B、H2SO4、H3PO4
C、SO2、NO D、Na2CO3、KClO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~D 是原子序数在 20 以内的元素,其性质或结构信息如下表:

请根据表中的信息回答下列问题:
(1)C 离子的结构示意图:_____________,B 原子的电子式:______________。
(2)写出和 B 的氢化物所含电子数相同的 3 种复杂微粒,这三种微粒分别是: 阴离子:_____,阳离子____________,电中性微粒:_____________。
(3)A 元素与 D 元素组成的化合物有非常重要的用途,写出实验室制备该气体的化学方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲是VIA族元素,其单质和化合物在化工生产等方面具有广泛地应用。
(1)TeO2是两性氧化物,微溶于水,可溶于强酸或强碱。TeO2和NaOH溶液发生反应的离子方程式为_________________________________。
(2)碲酸(H6TeO6)是一种很弱的酸,Ka1=1×10-7,该温度下,0.1mol/L H6TeO6的电离度a为_____________(结果保留1位有效数字)。
(3)从粗铜精练的阳极泥(主要含有Cu2Te)中提取粗碲的一种工艺流程如图:

①已知加压酸浸时控制溶液的pH为5.0,生成TeO2沉淀。如果H2SO4溶液浓度过大,产生的后果是____________________________。
②“加压酸浸”中为什么要加压?_______________________________。
③对滤渣“酸浸”后,将Na2SO3加入Te(SO4)2溶液中进行“还原”得到固态碲,该反应的离子方程式是_________________________________。
④“还原”得到固态碲后分离出粗碲的方法是_______,对粗碲进行洗涤,判断洗涤干净的实验操作和现象是______________________________________。
已知阳极泥中Cu2Te的含量为a%,则m吨阳极泥理论上可制得纯度为n%的粗碲___吨。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com