
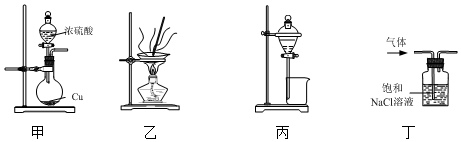
| A. | 用装置甲制取少量SO2 | |
| B. | 用装置乙蒸发FeCl3溶液制取FeCl3晶体 | |
| C. | 用装置丙分离CH3COOH和CH3COOCH2CH3的混合液 | |
| D. | 用装置丁除去Cl2中混有的少量HCl气体 |
分析 A.浓硫酸和铜常温下不反应;
B.FeCl3溶液在加热时易水解;
C.CH3COOH和CH3COOCH2CH3不分层;
D.氯气不溶于饱和食盐水.
解答 解:A.浓硫酸和铜常温下不反应,应在加热条件下进行,故A错误;
B.FeCl3溶液在加热时易水解,加热生成氢氧化铁,应在氯化氢的氛围中加热蒸发,故B错误;
C.CH3COOH和CH3COOCH2CH3混溶,二者沸点不同,可用蒸馏的方法分离,故C错误;
D.氯气不溶于饱和食盐水,可用洗气的方法除杂,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的制备、分离等,把握实验原理及实验装置图的作用为解答的关键,注意方案的合理性、操作性分析,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 50mL18mol•L-1浓硫酸与足量铜供热,转移电子数为0.9NA | |
| C. | 0.1molCl2通入含0.1molFeBr2溶液中,被氧化的溴离子数为0.2NA | |
| D. | 标准状况下,2.24LNO和足量O2反应生成物中含有NO2分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)=0.1 mo1•L-1 | B. | c(CO32-)>c(OH-) | ||
| C. | c(HCO3-)>c(CO32-) | D. | c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
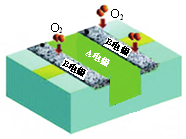
| A. | 电池工作时,电子由A电极经外电路流向B电极 | |
| B. | 电池工作时,减少的化学能完全转化为电能 | |
| C. | A电极发生的电极反应为:CH3OH-6e-+H2O═CO2+6H+ | |
| D. | B电极每消耗1 mol O2,电池中减少4 mol H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCO3可以除去MgCl2酸性溶液中的Fe3+ | |
| B. | 实验测得NaHSO3溶液的pH<7,说明则H2SO3是强酸 | |
| C. | 通过化学变化可以“点石成金”,即可将黏土转化成金单质 | |
| D. | 2.24LNO与1.12O2充分反应所得气体中原子数目一定为0.3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱石灰具有吸水性,可用于干燥氯气 | |
| B. | 甲醛能使蛋白质变性,可以用于食品防腐剂 | |
| C. | 炭具有强还原性,常用于冶炼钠、钾等金属 | |
| D. | 碳酸氢钠溶液具有弱碱性,可用于制胃酸中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com