
| A. | 常温常压下,2.24 LSO2中所含氧原子数为0.2NA | |
| B. | 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA | |
| C. | 1 mol NO2与足量H2O反应,转移的电子数为NA | |
| D. | 0.1 mol熔融的NaHSO4中阳离子数目为0.lNA |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、氯气和水反应是可逆反应;
C、二氧化氮和水的反应中,3mol二氧化氮转移2mol电子;
D、硫酸氢钠在熔融状态下电离为钠离子和硫酸氢根离子.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故2.24L二氧化硫的物质的量小于0.1mol,故含有的原子个数小于0.2NA个,故A错误;
B、氯气和水反应是可逆反应,在氯水中含氯气分子、HCl和HClO,故溶液中的N(HC1O)+N(Cl-)+N(ClO-)+2N(Cl2)=2NA,故B错误;
C、二氧化氮和水的反应中,3mol二氧化氮转移2mol电子,故1mol二氧化氮转移$\frac{2}{3}$NA个电子,故C错误;
D、硫酸氢钠在熔融状态下电离为钠离子和硫酸氢根离子,故0.1mol硫酸氢钠中含0.1NA个阳离子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲烷是天然气的主要成分,能发生取代反应,但不能发生氧化反应 | |
| B. | 实验室中,可用金属钠检验乙醇中是否含有水 | |
| C. | 只用水无法鉴别苯、乙酸和四氯化碳 | |
| D. | 植物油不能用于萃取溴水中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我国古代四大发明之一黑火药由硫酸、硝酸和木炭按一定比例混合制成 | |
| B. | PH计不能用于酸碱中和滴定终点的判断 | |
| C. | 石油的分馏,煤的干馏、气化、液化均是物理变化 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操作 | 现象 |
| Ⅰ.向盛有4.0gNa2O2的烧杯中加入50mL蒸馏水 | 剧烈反应,产生的气体能使带火星木条复燃,固体全部溶解后,得到的无色溶液a |
| Ⅱ.向溶液a中滴入两滴酚酞 | 溶液变红,10分钟后溶液颜色明显变浅,稍后,溶液变为无色 |
| Ⅲ.向溶液中加入少量MnO2粉末 | 又有大量气泡产生,产生的气体也能使带火星木条复燃 |
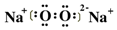 ,很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表
,很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表查看答案和解析>>
科目:高中化学 来源: 题型:解答题
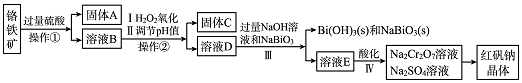
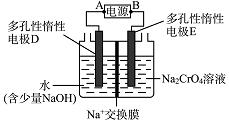
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 78g苯中含有的碳碳双键的数目为3NA | |
| B. | 16g由Cu2S和CuO组成的混合物中含有的阳离子数为0.2NA | |
| C. | 将1molH2与1molI2充入一密闭容器中充分反应后,转移的电子数为2NA | |
| D. | 1mo1Fe与足量的浓硫酸共热反应,生成SO2的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C≡C | H-O | C-H |
| E/(KJ.mol-1) | 436 | 343 | x | 465 | 413 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属原子间以共价键结合的物质一定是共价化合物 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | 凡是能电离出离子的化合物一定是离子化合物 | |
| D. | 凡是含有离子键的化合物一定是离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com