
(综合应用)用含FeS280%的硫铁矿生产硫酸,已知该矿石的燃烧率为95%,SO2的转化率为90%,SO3的吸收率为98%。若生产500 t98%的硫酸,需矿石的质量和标准状况下空气的体积(假设空气中氧 的体积分数为20%)是多少?
点拨解答:此题涉及到多步连续反应的计算,若采用相当量关系式的方法,则把各步反应的转化率当成原料的有效成分含量。特别注意的是:氧气参与了两个反应,在找氧气和H2SO4的关系式时,不可漏掉任何一步反应所消耗的氧气。 设需要矿石的质量为m,氧气物质的量为n。由反应的化学方程式可得: FeS2 ~ 2H2SO4 120 196 m·80%·95%·90%·98% 500t·98% 解之得:m=447.5t 15O2 ~ 8H2SO4 15mo1 784g n 500t·98%·106g 解之得:n=9.38X106mol 所需空气的体积为 V=9.38×l06mol×22.4 L·mol-1÷20%=1.05Xl09L。
|


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:阅读理解

| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 |
 MnS2O6的△H
MnS2O6的△H查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
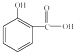 (1)食品和药品关系人的生存和健康.
(1)食品和药品关系人的生存和健康.

| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com