
ĻĀĮŠø÷×éŌ×Ó£¬±Ė“ĖŠŌÖŹŅ»¶ØĻąĖʵďĒ£Ø””””£©
”” A£® 1s2Óė2s2µÄŌŖĖŲ
”” B£® M²ćÉĻÓŠĮ½øöµē×ÓÓėN²ćÉĻÓŠĮ½øöµē×ÓµÄŌŖĖŲ
”” C£® 2pÉĻÓŠŅ»øöĪ“³É¶Ōµē×ÓÓė3pÉĻÓŠŅ»øöĪ“³É¶Ōµē×ÓµÄŌŖĖŲ
”” D£® L²ćÉĻÓŠŅ»øöæÕ¹ģµĄŗĶM²ćµÄp¹ģµĄÉĻÓŠŅ»øöæÕ¹ģµĄµÄŌŖĖŲ
æ¼µć£ŗ Ō×ÓŗĖĶāµē×ÓÅŲ¼£®
×ØĢā£ŗ Ō×Ó×é³ÉÓė½į¹¹×ØĢā£®
·ÖĪö£ŗ A.1s2ĪŖHe£¬ŠŌÖŹĪČ¶Ø£¬2s2µÄŌŖĖŲĪŖBe£¬ŠŌÖŹ½Ļ»īĘĆ£»
B£®M²ćÉĻÓŠĮ½øöµē×ÓĪŖMg£¬N²ćÉĻÓŠĮ½øöµē×ÓµÄŌŖĖŲĪŖCa»ņĘäĖüµŚĖÄÖÜĘŚŹĒ¹ż¶É½šŹōŌŖĖŲ£»
C.2pÉĻÓŠŅ»øöĪ“³É¶Ōµē×Ó£¬ĪŖ2p1»ņ2p5£¬æÉÄÜĪŖB»ņF£»3pÉĻÓŠŅ»øöĪ“³É¶Ōµē×ÓµÄŌŖĖŲ£¬æÉÄÜĪŖAl»ņCl£»
D£®L²ćÉĻÓŠŅ»øöæÕ¹ģµĄ£¬µē×ÓÅŲ¼ĪŖ1s22s22p2£¬ŌņĪŖC£»M²ćµÄp¹ģµĄÉĻÓŠŅ»øöæÕ¹ģµĄ£¬µē×ÓÅŲ¼ĪŖ1s22s22p63s23p2£¬ŌņĪŖSi£®
½ā“š£ŗ ½ā£ŗA.1s2ĪŖHe£¬ŠŌÖŹĪČ¶Ø£¬2s2µÄŌŖĖŲĪŖBe£¬ŠŌÖŹ½Ļ»īĘĆ£¬¶žÕߊŌÖŹŅ»¶Ø²»ĻąĖĘ£¬¹ŹA“ķĪó£»
B£®M²ćÉĻÓŠĮ½øöµē×ÓĪŖMg£¬N²ćÉĻÓŠĮ½øöµē×ÓµÄŌŖĖŲĪŖCa»ņĘäĖüµŚĖÄÖÜĘŚŹĒ¹ż¶É½šŹōŌŖĖŲ£¬¶žÕߊŌÖŹæÉÄÜĻąĖĘ£¬¹ŹB“ķĪó£»
C.2pÉĻÓŠŅ»øöĪ“³É¶Ōµē×Ó£¬ĪŖ2p1»ņ2p5£¬æÉÄÜĪŖB»ņF£»3pÉĻÓŠŅ»øöĪ“³É¶Ōµē×ÓµÄŌŖĖŲ£¬æÉÄÜĪŖAl»ņCl£¬ČōĪŖĶ¬Ö÷×åŌŖĖŲ£¬ŠŌÖŹĻąĖĘ£¬Čō²»Ķ¬Ö÷×åŹ±£¬ŠŌÖŹ²»ĻąĖĘ£¬¹ŹC“ķĪó£»
D£®L²ćÉĻÓŠŅ»øöæÕ¹ģµĄ£¬µē×ÓÅŲ¼ĪŖ1s22s22p2£¬ŌņĪŖC£»M²ćµÄp¹ģµĄÉĻÓŠŅ»øöæÕ¹ģµĄ£¬µē×ÓÅŲ¼ĪŖ1s22s22p63s23p2£¬ŌņĪŖSi£¬C”¢SiĪ»ÓŚĶ¬Ņ»Ö÷×壬ŠŌÖŹŅ»¶ØĻąĖĘ£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ£ŗ ±¾Ģāæ¼²éµē×ÓÅŲ¼ÓėĶ¬Ö÷×åŌŖĖŲŠŌÖŹµÄĻąĖĘŠŌ£¬ĄūÓƵē×ÓÅŲ¼ĶĘ³öŌŖĖŲŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬ŹģĻ¤µē×ÓÅŲ¼¹ęĀɼ“æɽā“š£¬ĢāÄæÄѶČÖŠµČ£®
””



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
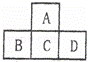
ÓŠA”¢B”¢C”¢D”¢EĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ŅŃÖŖĻąĮŚµÄA”¢B”¢C”¢DĖÄÖÖŌŖĖŲµÄŌ×ÓŗĖĶā¹²ÓŠ56øöµē×Ó£¬ŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼ĖłŹ¾£®EŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¼ČÄÜÓėĒæĖį·“Ó¦ÓÖÄÜÓėĒæ¼ī·“Ó¦£®Ēė»Ų“š£ŗ
£Ø1£©Š“³öĻĀĮŠŌŖĖŲµÄŌŖĖŲ·ūŗÅ£ŗA”””””¢B”””””¢D””£®
£Ø2£©AŌŖĖŲÓėĒāŌŖĖŲŠĪ³ÉµÄH2A»ÆŗĻĪļ·Ö×ÓÖŠ£¬Ėłŗ¬»Æѧ¼üĪŖ””””¼ü£ØĢī”°Ąė×Ó”±»ņ”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±£©£¬ÓƵē×ÓŹ½±ķŹ¾H2AµÄŠĪ³É¹ż³Ģ””£¬””£®
£Ø3£©AŌŖĖŲÓėEŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒ””””£¬øĆ»ÆŗĻĪļŌŚĪļÖŹ·ÖĄąÖŠŹōÓŚ””””Ńõ»ÆĪļ£®£ØĢī”°ĖįŠŌ”±£¬”°¼īŠŌ”±»ņ”°Į½ŠŌ”±£©
£Ø4£©ĻņDŌŖĖŲÓėEŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļµÄĖ®ČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗ£¬æŖŹ¼Ź±£¬ŹµŃéĻÖĻóŹĒ””ÓŠ””£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ””””£»¼ĢŠųµĪ¼ÓNaOHČÜŅŗÖĮ¹żĮ棬ŹµŃéĻÖĻóŹĒ””””£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
25”ꏱ£¬ŃĪĖįČÜŅŗµÄpHŹĒ4£¬ĀČ»Æļ§ČÜŅŗµÄpHŹĒ5£¬ŃĪĖįÓėĀČ»Æļ§ČÜŅŗÖŠĖ®µēĄėµÄc£ØH+£©Ö®±ČĪŖ£Ø£©
A£® 10£ŗ1 B£® 1£ŗ10 C£® 1£ŗ105 D£® 105£ŗ1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½ūÖ¹Ź¹ÓĆŠĖ·Ü¼ĮŹĒ°ĀŌĖ»į±£Ö¤ŌĖ¶ÆŌ±±ČČü¹«Ę½µÄÖŲŅŖ¾Ł“ėÖ®Ņ»£®ŅŌĻĀĮ½ÖÖŠĖ·Ü¼Į½į¹¹·Ö±šĪŖ£ŗ

Ōņ¹ŲÓŚĖüĆĒµÄĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
”” A£® ĄūÄņĖį·Ö×ÓÖŠÓŠČżÖÖ¹ŁÄÜĶÅ
”” B£® Į½ÖÖ·Ö×ÓÖŠµÄĖłÓŠĢ¼Ō×Ó¾ł²»æÉÄܹ²Ę½Ćę
”” C£® Į½ÖÖŠĖ·Ü¼Į¾łŹōÓŚ·¼ĻćĢž
”” D£® Į½ÖÖ·Ö×Ó¾łæÉ·¢Éś¼Ó³É·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
×ī½ü£¬Ć½Ģå±ØµĄ²»·ØÉĢ··ĻśŹŪ”°ÖĀ°©“óĆ×”±£¬ŅŃŃéÖ¤ÕāÖÖ“óĆ×ÖŠŗ¬ÓŠ»ĘĒśĆ¹¶¾ĖŲ£ØAFTB£©£¬Ęä·Ö×Ó½į¹¹Ź½ĪŖČēĶ¼ĖłŹ¾£¬ČĖĢåµÄĢŲŹā»łŅņŌŚ»ĘĒśĆ¹ĖŲµÄ×÷ÓĆĻĀ»į·¢ÉśĶ»±ä£¬ÓŠ×Ŗ±äĪŖøĪ°©µÄæÉÄÜ£®Ņ»°ćĢõ¼žĻĀøś1mol AFTBĘš·“Ó¦µÄH2»ņNaOHµÄ×ī“óĮæ·Ö±šŹĒ£Ø””””£©
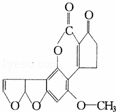
”” A£® 6mol£»1mol B£® 5mol£»1mol C£® 6mol£»2mol D£® 5mol£»2mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
X”¢Y”¢Z”¢Q”¢EĪåÖÖŌŖĖŲÖŠ£¬XŌ×ÓŗĖĶāµÄM²ćÖŠÓŠ2øöµ„µē×ÓĒŅÓėZĶ¬Ö÷×壬YŌ×ÓŗĖĶāµÄL²ćµē×ÓŹżŹĒK²ćµÄĮ½±¶£¬ZŹĒµŲæĒÄŚŗ¬Įæ£ØÖŹĮæ·ÖŹż£©×īøßµÄŌŖĖŲ£¬QµÄŗĖµēŗÉŹżŹĒXÓėZµÄŗĖµēŗÉŹżÖ®ŗĶ£¬EŌŚŌŖĖŲÖÜĘŚ±ķµÄø÷ŌŖĖŲÖŠµēøŗŠŌ×ī“ó£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©X”¢YµÄŌŖĖŲ·ūŗÅŅĄ“ĪĪŖ”””””¢””””£»
£Ø2£©YZ2·Ö×ÓµÄĮ¢Ģå½į¹¹ŹĒ””””£»
£Ø3£©QµÄŌŖĖŲ·ūŗÅŹĒ””””£¬ĖüµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ””””£¬ŌŚŠĪ³É»ÆŗĻĪļŹ±ĖüµÄ×īøß»ÆŗĻ¼ŪĪŖ””””£»
£Ø4£©EµÄĒā»ÆĪļµÄČŪ·Šµć±ČĶ¬×åĘäĖüŌŖĖŲĒā»ÆĪļµÄČŪ·Šµć¶¼ŅŖøßŗܶą£¬ŌŅņŹĒ””HF·Ö×Ó¼ä“ęŌŚ””
£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚĻąĶ¬Ģõ¼žĻĀ£¬ĻĀĮŠČżøö»Æѧ·“Ó¦·Å³öµÄČČĮæ·Ö±šŅŌ”÷H1”¢”÷H2”¢”÷H3±ķŹ¾£ŗ
£Ø1£©2H2£Øg£©+O2£Øg£©═2H2O£Øg£©”÷H1
£Ø2£©2H2£Øg£©+O2£Øg£©═2H2O£Øl£©”÷H2
£Ø3£©H2£Øg£©+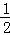 O2£Øg£©═H2O£Øg£©”÷H3
O2£Øg£©═H2O£Øg£©”÷H3
Ōņ”÷H1”¢”÷H2ŗĶ”÷H3µÄ¹ŲĻµŹĒ£Ø£©
A£® ”÷H1=”÷H2=”÷H3 B£® ”÷H1£¼”÷H2£¬”÷H3=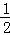 ”÷H1
”÷H1
C£® ”÷H1£¾”÷H2£¬”÷H2=2”÷H3 D£® ĪŽ·Ø±Č½Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øĒĖ¹¶ØĀÉŌŚÉś²śŗĶæĘѧъ¾æÖŠÓŠŗÜÖŲŅŖµÄŅāŅ壮ӊŠ©·“Ó¦µÄ·“Ó¦ČČĖäČ»ĪŽ·ØÖ±½Ó²āµĆ£¬µ«æÉĶعż¼ä½ÓµÄ·½·Ø²ā¶Ø£®ĻÖøł¾ŻĻĀĮŠ3øöČČ»Æѧ·“Ó¦·½³ĢŹ½£ŗ
Fe2O3£Øs£©+3CO£Øg£©=2Fe£Øs£©+3CO2£Øg£©”÷H=﹣24.8kJ/mol
3Fe2O3£Øs£©+CO£Øg£©=2Fe3O4£Øs£©+CO2£Øg£©”÷H=﹣47.2kJ/mol
Fe3O4£Øs£©+CO£Øg£©=3FeO£Øs£©+CO2£Øg£©”÷H=+640.5kJ/mol
Š“³öCOĘųĢ廹ŌFeO¹ĢĢåµĆµ½Fe¹ĢĢåŗĶCO2ĘųĢåµÄČČ»Æѧ·“Ó¦·½³ĢŹ½£ŗ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
I.½«0.40mol N2O4ĘųĢå³äČė2 L¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ·¢ÉśČēĻĀ·“Ó¦£ŗN2O4(g) 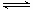 2NO2(g) ”÷H”£ŌŚTl”ęŗĶT2”ꏱ£¬²āµĆNO2µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆČēĻĀĶ¼ĖłŹ¾£ŗ
2NO2(g) ”÷H”£ŌŚTl”ęŗĶT2”ꏱ£¬²āµĆNO2µÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆČēĻĀĶ¼ĖłŹ¾£ŗ
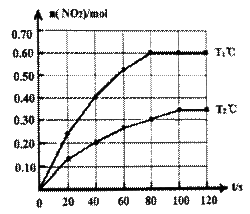
(1)Tl”ꏱ£¬40s”«80sÄŚÓĆN2O4±ķŹ¾øĆ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ_________________mol/(L·s)”£
(2)”÷H___________0(Ģī”°>”±”¢”°<”±»ņ”°=”±)”£
(3)øıäĢõ¼žÖŲŠĀ“ļµ½Ę½ŗāŹ±£¬ŅŖŹ¹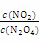 µÄ±ČÖµ±äŠ”£¬æɲÉČ”µÄ“ėŹ©ÓŠ__________(ĢīŠņŗÅ)”£
µÄ±ČÖµ±äŠ”£¬æɲÉČ”µÄ“ėŹ©ÓŠ__________(ĢīŠņŗÅ)”£
a.Ōö“óN2O4µÄĘšŹ¼ÅØ¶Č b.ÉżøßĪĀ¶Č
c.Ļņ»ģŗĻĘųĢåÖŠĶØČėNO2 d.Ź¹ÓĆøߊ§“߻ƼĮ
II.ŅŃÖŖ£ŗ³£ĪĀĻĀ£¬HCNµÄµēĄė³£ŹżĪŖKa=5”Į10£10”£
(4)ÓŠÅضČĻąĶ¬µÄHCNŗĶNaCNµÄ»ģŗĻČÜŅŗ”£
¢ŁĶعż¼ĘĖćĖµĆ÷øĆČÜŅŗµÄĖį¼īŠŌ_____________________________________________”£
¢ŚøĆČÜŅŗÖŠø÷Ąė×ÓµÄÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ___________________________________”£
(5)³£ĪĀĻĀ£¬ĻņijÅØ¶ČµÄHCNČÜŅŗÖŠÖšµĪ¼ÓČėNaOHČÜŅŗÖĮČÜŅŗ³ŹÖŠŠŌ”£
¢ŁøĆ¹ż³ĢČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČµÄ±ä»ÆĪŖ______________”£
¢ŚČō»ģŗĻČÜŅŗÖŠc(Na+)=a mol/L£¬Ōņc(HCN)=_________mol/L”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com