
| 混合物 | 试剂 | 分离方法 | |
| A | 溴苯(溴) | 氢氧化钠溶液 | 过滤 |
| B | 苯(甲苯) | 酸性高锰酸钾溶液 | 分液 |
| C | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
| D | 溴乙烷(乙醇) | 蒸馏水 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溴与NaOH溶液反应后,与溴苯分层;
B.甲苯被高锰酸钾氧化生成苯甲酸,与苯不分层;
C.乙酸与碳酸钠反应后,与乙酸乙酯分层;
D.乙醇易溶于水,与溴乙烷分层.
解答 解:A.溴与NaOH溶液反应后,与溴苯分层,然后利用分液法分离,故A不选;
B.甲苯被高锰酸钾氧化生成苯甲酸,与苯不分层,应选择蒸馏法分离,故B不选;
C.乙酸与碳酸钠反应后,与乙酸乙酯分层,然后利用分液法分离,故C选;
D.乙醇易溶于水,与溴乙烷分层,然后利用分液法分离,故D选;
故选CD.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法的选择为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| 二甲苯一溴代物的熔点/℃ | 234 | 206 | 213 | 204 | 214 | 205 |
| 对应的二甲苯的熔点/℃ | 13 | -54 | -27 | -54 | -27 | -54 |
| A. | 熔点为234℃的是一溴代间二甲苯 | B. | 熔点为234℃的是一溴代邻二甲苯 | ||
| C. | 熔点为-54℃的是间二甲苯 | D. | 熔点为-27℃的是对二甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
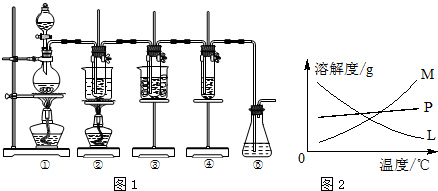
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素单质的最外层电子数都是7 | |
| B. | 从上到下,卤素原子的电子层数依次增多,半径依次减小 | |
| C. | 卤素单质与H2化合的容易程度为F2<Cl2<Br2<I2 | |
| D. | 从F到I,原子核对最外层电子的吸引能力依次减弱,原子得电子能力依次减弱,元素的非金属性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状态下,1L庚烷完全燃烧后,所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 1mol碳正离子CH5+所含的电子数为11NA | |
| C. | 标准状态下,16g甲烷完全燃烧所消耗的氧气的分子数为2NA | |
| D. | 0.5molC3H8分子中含C-H共价键2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙醛 | B. | 丁醛 | C. | 己醛 | D. | 3-甲基丁醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
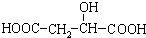 )广泛存在于水果中,尤以苹果、葡萄、西瓜、山
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山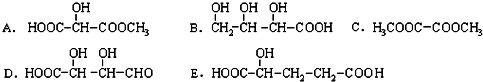
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定无Na2CO3,可能有FeCl3 | B. | 一定有MgCl2,一定无NaCl | ||
| C. | 一定有MgCl2,可能有Na2CO3 | D. | 一定有MgCl2,可能有NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
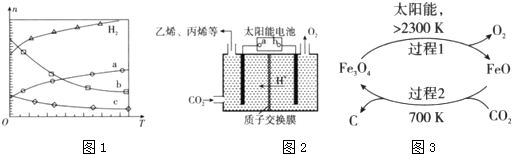
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com