
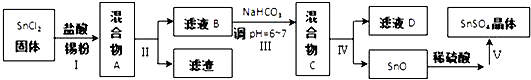
���� ����Sn2+��ˮ�⡢�ױ��������������ᣬ����Sn2+ˮ�⣬����Sn�ۿ��������ᷴӦ��������ҺpH������ֹSn2+�������������Ϊ���ˣ���SnCl2��Һ�������м�̼�����ƣ�������ҺpH��ʹMnԪ����SnO��ʽ�������ٹ���ϴ�ӵô�����SnO����ϡ���ᣬ��SnSO4��Һ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ��Ƶ�SnSO4���壬��ҺD�к��д�����NaCl�ȣ�
��1���ټ���Sn�ۿ��������ᷴӦ��������ҺpH������ֹSn2+��������
�ڵõ�������SnO��SnԪ�ػ��ϼ�Ϊ�仯�����ڷ�������ԭ��Ӧ�����ʷ���ˮ�ⷴӦ����Sn��OH��2�������̼��Sn��OH��2����ˮ�õ�SnO��
�ܳ���ΪSnO���渽����Cl-��Ҫ����������Ƿ�ϴ�Ӹɾ��������ᡢ��������Һ�������һ��ϴ��Һ���Ƿ���Cl-��
��2��SnCl4ˮ��õ�Sn��OH��4��HCl��HCl�백����Ӧ�õ�NH4Cl��
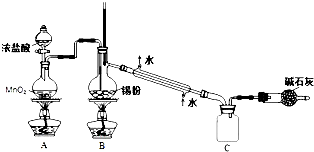
����SnCl4��ˮ�⣬�Ʊ���Ӧ�ڸ��ﻷ���н��У��Ʊ��������к���HCl��ˮ��������Ҫ��ȥ����ֹSn��HCl��Ӧ��SnCl4ˮ�⣻
���������������ϵķ�Ӧ�Ƿ��ȷ�Ӧ���ҷų������㹻�˷�Ӧ�������У�
��3��SnCl4����ˮ�⡢�۵�Ϊ-33�桢�е�Ϊ114�棬ȡ2.5g������Ʒ��������ַ�Ӧ��Cƿ��ֵ5.22gΪSnCl4�����������Ԫ���غ�������Ĵ��ȣ�
��� �⣺��1��������Ϣ��֪��Sn2+�ױ�����������Sn�۳�������ҺpH�⣬����ֹSn2+��������������ҺpH��
�ʴ�Ϊ����ֹSn2+��������
�ڵõ�������SnO��SnԪ�ػ��ϼ�Ϊ�仯�����ڷ�������ԭ��Ӧ�����ʷ���ˮ�ⷴӦ����Sn��OH��2�������̼��Sn��OH��2����ˮ�õ�SnO����Ӧ���ӷ���Ϊ��Sn2++2HCO3-=SnO��+2CO2��+H2O��
�ʴ�Ϊ��Sn2++2HCO3-=SnO��+2CO2��+H2O��
��������ͼ��֪������V�Ǵ���Һ�еõ����ᾧˮ�ľ��壬ֻ�ܲ�ȡ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵõ���
�ʴ�Ϊ������Ũ������ȴ�ᾧ��
��2��SnCl4ˮ��õ�Sn��OH��4��HCl��HCl�백����Ӧ�õ�NH4Cl����Ӧ����ʽΪ��SnCl4+4NH3+4H2O=Sn��OH��4+4NH4Cl��
����SnCl4��ˮ�⣬�Ʊ���Ӧ�ڸ��ﻷ���н��У��Ʊ��������к���HCl��ˮ��������Ҫ��ȥ����ֹSn��HCl��Ӧ��SnCl4ˮ�⣬�Ľ������ǣ���A��Bװ�ü���������ʢ�б���ʳ��ˮ��Ũ�����ϴ��ƿ��
���������������ϵķ�Ӧ�Ƿ��ȷ�Ӧ���ҷų������㹻�˷�Ӧ�������У�
�ʴ�Ϊ����A��Bװ�ü���������ʢ�б���ʳ��ˮ��Ũ�����ϴ��ƿ�����������������ϵķ�Ӧ�Ƿ��ȷ�Ӧ���ҷų������㹻�˷�Ӧ�������У�
��3��ȡ2.5g������Ʒ��������ַ�Ӧ��Cƿ��ֵ5.22gΪSnCl4�����������ʵ���=$\frac{5.22g}{261g/mol}$=0.02mol��
����Ʒ����=$\frac{0.02mol��119g/mol}{2.5g}$��100%=95.2%��
�ʴ�Ϊ��95.2%��
���� ��������ƴ������Ŀ���漰�����Ʊ���������ѧ�������̡����ʺ����ⶨ��Ԫ�����ڱ���Ԫ�������ɵȣ��Ƕ�ѧ���ۺ������Ŀ��飬��Ҫѧ���߱���ʵ�Ļ��������õ��������ʣ���Ŀ�Ѷ��еȣ�


 ���100��1�ž�ϵ�д�
���100��1�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
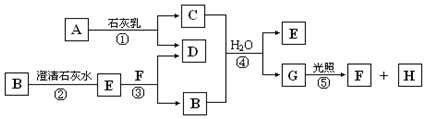 ͼ��A��H��Ϊ��ѧ��ѧ�г��������ʣ�A��B��H�����壬����֮������ͼת����ϵ����Ӧ�����ɵ�ˮ����ȥ����
ͼ��A��H��Ϊ��ѧ��ѧ�г��������ʣ�A��B��H�����壬����֮������ͼת����ϵ����Ӧ�����ɵ�ˮ����ȥ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
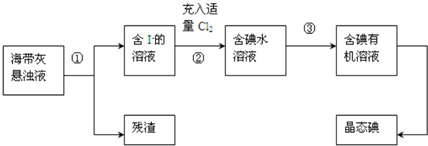
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BaCl2��Na2CO3��NaOH������ | B�� | NaOH��BaCl2��Na2CO3������ | ||
| C�� | Na2CO3��NaOH��BaCl2������ | D�� | BaCl2��NaOH��Na2CO3������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
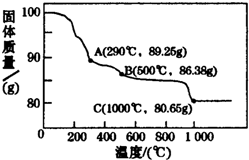 �ܣ�Co�����仯�����ڴ��Բ��ϡ���ز��ϡ���Ӳ���ϼ������������й㷺Ӧ�ã���֪��������ϵԪ�أ��䵥���뻯����������������ƣ��䳣�����ϼ���+2��+3����ش��������⣺
�ܣ�Co�����仯�����ڴ��Բ��ϡ���ز��ϡ���Ӳ���ϼ������������й㷺Ӧ�ã���֪��������ϵԪ�أ��䵥���뻯����������������ƣ��䳣�����ϼ���+2��+3����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
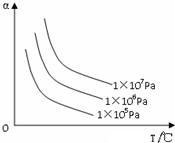
| A�� | C��s��+CO2��g��?2CO��g������H��0 | B�� | H2��g��+Br2��g��?2HBr��g������H��0 | ||
| C�� | N2��g��+3H2��g��?2NH3��g������H��0 | D�� | 2SO3��g��?2SO2��g��+O2��g������H��0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com