
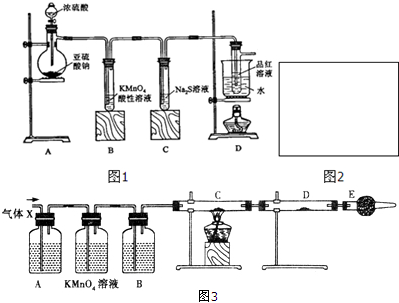
| A�� | ���Թ�ȡ���Լ�ƿ�е�Na2CO3��Һ������ȡ�����࣬Ϊ�˲��˷ѣ��ְѹ������Լ������Լ�ƿ�� | |
| B�� | Ba��NO3��2����ˮ���ɽ�����Ba��NO3��2�ķ�Һ����ˮ���У�����ˮ������ˮ�� | |
| C�� | ����������ʹNaCl ����Һ������ʱ��Ӧ����������NaCl ��Һȫ���������� | |
| D�� | ��Ũ��������һ�����ʵ���Ũ�ȵ�ϡ����ʱ��Ũ��������ˮ��Ӧ��ȴ�����²���ת�Ƶ�����ƿ�� |
���� A��ʣ��ҩƷ�������ⶪ����Ҳ���ܷŻ�ԭƿ��Ӧ�÷���ָ�������У�
B����ѧʵ��ķ�Һ�������ⶪ����Ӧ����ָ���������У�
C�������ᾧ���У�������ˮʱ�����ɽ�Һ�����ɣ�
D��Ũ��������ˮ�ų������ȣ��ȵ���Һ���ƫ������ȴ�����²���ת�Ƶ�����ƿ�У�����Ӱ�����ƽ����
��� �⣺A����ѧʵ��ʣ��ҩƷ���ɷŻ�ԭƿ���������ⶪ���������ó�ʵ���ң�Ӧ����ָ���������У���A����
B��������Ba��NO3��2�ķ�Һ�������ⶪ����Ӧ����ָ���������У���B����
C����������������ù���ķ�������ȼ�ƾ��Ƽ��ȣ������裬���н϶ྦྷ������ʱ��ֹͣ���ȣ����������ɣ���C����
D����Ũ��������һ�����ʵ���Ũ�ȵ�ϡ����ʱ��Ũ��������ˮ���ų�������Ӱ����Һ�����Ӧ����ȴ�����º�ת�Ƶ�����ƿ�У���D��ȷ��
��ѡD��
���� ���⿼���˻�ѧʵ����������������жϣ���Ŀ�ѶȲ���ѧ����ʵ��Ϊ������ѧ�ƣ���ȷ�Ļ�ѧ����ʵ�������ʵ��ɹ���ǰ��ͱ��ϣ�Ҫ��ѧ���������ճ�����ѧʵ���������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ���ĵ���ʽ�� | B�� | CO2�Ľṹʽ��O=C=O | ||
| C�� | �����ӽṹʾ��ͼ�� | D�� | CCl4�ĵ���ʽ��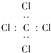 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
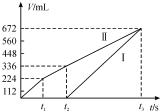 �������ö��Ե缫���200mLNaCl��CuSO4�Ļ����Һ����������������ʱ��仯��ͼ��ʾ������ͼ����Ϣ�ش��������⣬����������ѻ���ɱ�״���µ�������Һ���������ˮ�е��ܽ����Һ����ı仯��
�������ö��Ե缫���200mLNaCl��CuSO4�Ļ����Һ����������������ʱ��仯��ͼ��ʾ������ͼ����Ϣ�ش��������⣬����������ѻ���ɱ�״���µ�������Һ���������ˮ�е��ܽ����Һ����ı仯���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MgSO4 | B�� | FeCl2 | C�� | AlCl3 | D�� | NaAlO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | S��s��+O2��g��=SO2��g������Ӧ�ų�����������293.23 kJ•mol-1 | |
| B�� | S��g��+O2��g��=SO2��g������Ӧ�ų�������С��293.23 kJ•mol-1 | |
| C�� | 1 mol SO2��g���ļ��ܵ��ܺ�С��1 mol S��l����1 mol O2��g���ļ���֮�� | |
| D�� | 1 mol SO2��g���ļ��ܵ��ܺʹ���1 mol S��l����1 mol O2��g���ļ���֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ��������ľ̿���� | ||
| C�� | �ƾ�����ˮ | D�� | HCl��������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���Ṥҵβ���ж�������ĺ�������0.05%�����������ʱ�辭����������ŷţ�ijУ��ȤС�����ⶨ���Ṥҵβ���ж�������ĺ������������·�����
���Ṥҵβ���ж�������ĺ�������0.05%�����������ʱ�辭����������ŷţ�ijУ��ȤС�����ⶨ���Ṥҵβ���ж�������ĺ������������·������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com