
| A、新制氯水具有漂白作用 |
| B、新制氯水呈黄绿色 |
| C、新制氯水应避光保存 |
| D、氯水是指液态的氯 |
科目:高中化学 来源: 题型:
| A、发生化学反应时失去电子越多的金属原子,还原能力越强 |
| B、某元素从化合态变成游离态,该元素一定被还原 |
| C、由同种分子构成的物质一定是纯净物 |
| D、电离时能生成H+的化合物一定是酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2是硅酸的酸酐,可与水化合生成硅酸 |
| B、CO2通入水玻璃中可以得到硅酸 |
| C、在高温是SiO2与Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 |
| D、SiO2是酸性氧化物,它不溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)═2HBr(g)△H<0.当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是( )
在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)═2HBr(g)△H<0.当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是( )| A、若b、c点的平衡常数分别为K1、K2,则K1>K2 |
| B、a、b两点的反应速率:b>a |
| C、为了提高Br2(g)的转化率,可采取增加Br2(g)通入量的方法 |
| D、若平衡后保持温度不变,压缩容器体积平衡一定不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5.6g Fe与足量稀盐酸反应转移的电子数为0.3NA |
| B、常温常压下,23g NO2含有NA个氧原子 |
| C、标准状况下,22.4L水含有个NA H2O分子 |
| D、1mol/L NaCl溶液含有NA个Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
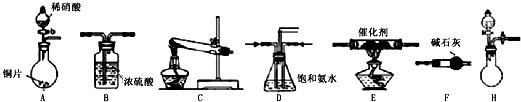
| 试剂组合序号 | 固体试剂 | NH3体积(mL) | |
| a | 6.0g Ca(OH)2(过量) | 5.4g NH4Cl | 1344 |
| b | 5.4g (NH4)2SO4 | 1364 | |
| c | 6.0g NaOH(过量) | 5.4g NH4Cl | 1568 |
| d | 5.4g (NH4)2SO4 | 1559 | |
| e | 6.0g CaO(过量) | 5.4g NH4Cl | 1753 |
| f | 5.4g (NH4)2SO4 | 1792 | |
 →
→查看答案和解析>>
科目:高中化学 来源: 题型:
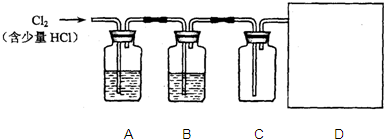
| 实验步骤 | 预期现象和相应结论 | |
| i |  试管B中的试剂为澄清石灰水.向试管A中滴入盐酸. 试管B中的试剂为澄清石灰水.向试管A中滴入盐酸. |
①若 ②若 |
| ii | 若“假设一”不成立,向实验步骤i反应后的试管A中滴入2滴 |
①若 中的②分析,则“假设三”成立. ②若 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在多电子的原子里,能量高的电子通常在离核近的区域内运动 |
| B、最外层电子数为8的微粒均是稀有气体元素的原子 |
| C、俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 |
| D、在周期表中金属和非金属的分界线附近寻找制备半导体材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com