
| A. | 含有大量Ba(NO3 )2的溶液中:Mg2+、NH4+、SO42-、Cl- | |
| B. | 无色透明的溶液中:Cu2+、K+、SO42-、NO3- | |
| C. | 在碱性溶液中:Na+、K+、SO42-、CO32- | |
| D. | 在酸性的溶液中:Na+、K+、CO32-、NO3- |
科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、NO3-、HCO3- | ||
| C. | SO42-、Fe3+、K+、Cl- | D. | NO3-、K+、SO32-、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH相等的四种溶液:a.CH3COONa b.C6H5ONa c.NaHCO3 d.NaOH,则四种溶液的溶质的物质的量浓度由小到大顺序为:d<b<c<a | |
| B. | pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | pH=2的一元酸和pH=12的二元强碱等体积混合:c(OH-)≤c(H+) | |
| D. | pH=4浓度均为0.1mol•L-1的CH3COOH、CH3COONa混合溶液中:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH2+HCl$→_{△}^{催化剂}$CH3CH2Cl | |
| B. | 2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH | |
| C. |  +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$ -Br+HBr -Br+HBr | |
| D. | CH3CH2Br+NaOH$→_{△}^{乙醇}$CH2═CH2↑+NaBr+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe | B. | K2CO3 | C. | KOH | D. | ZnCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
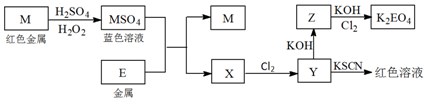
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 21:5 | B. | 11:3 | C. | 1:4 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
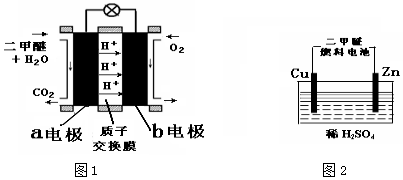
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com