
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 钠 | 镁 | 铝 | 硅 |
| 电负性 | 0.9 | 1.2 | x | 1.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 金属的用途 | 对应的金属物理性质 |
| 用铝定制成包装用的铝箔 | |
| 用铁、铝等做炊具 | |
| 用铜与氯化铁溶液反应制作印刷电路 | |
| 电信业中大量使用的铜丝、金属电缆 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
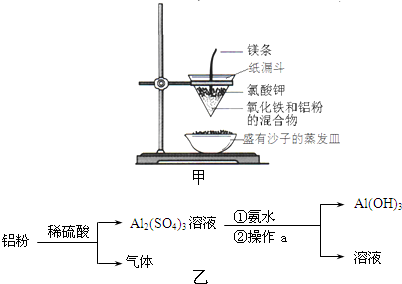
查看答案和解析>>
科目:高中化学 来源:必修一导学指导化学鲁科版 鲁科版 题型:043
《拯救大兵瑞恩》里面有一个美军用燃烧弹烧死坑道中敌兵的镜头,这就是燃烧弹在现代坑道战、堑壕战中的作用之一.由于汽油密度较小,发热量高,便宜,所以被广泛用作燃烧弹原料.加入能与汽油结合成胶状物的黏合剂,就制成了凝固汽油弹.为了攻击水中目标,有的还在凝固汽油弹里添加活泼碱金属和碱土金属钾、钙、钡,金属与水结合放出的氢气又发生燃烧,提高了燃烧威力.
对于有装甲的坦克,燃烧弹自有对付的高招,由于铝粉和氧化铁能发生壮观的铝热反应,2Al+Fe2O3![]() Al2O3+2Fe+热量,该反应放出的热量足以使钢铁熔化成液态,所以用铝热剂制成的燃烧弹可熔掉坦克厚厚的装甲,使其望而生畏.
Al2O3+2Fe+热量,该反应放出的热量足以使钢铁熔化成液态,所以用铝热剂制成的燃烧弹可熔掉坦克厚厚的装甲,使其望而生畏.
问题1:对于上述材料中的铝热反应,从各个角度分析其反应类型.
问题2:用图示表示出四个基本反应类型与氧化还原反应、非氧化还原反应的关系.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com