
下列反应过程中,同时有离子键、极性键和非极性键的断裂和形成的是
A.NH4Cl  NH3↑+HCl↑ B.NH3+CO2+H2O===NH4HCO3
NH3↑+HCl↑ B.NH3+CO2+H2O===NH4HCO3
C.2Na2O2+2H2O===4NaOH+O2 ↑ D.2NaOH+Cl2===NaCl+NaClO+H2O
科目:高中化学 来源: 题型:
将下列各种液体①苯 ②四氯化碳 ③碘化钾溶液 ④己烯,分别与溴水混合后充分振荡、静置,液体分为两层,原溴水层几乎是无色的是( )
A.只有② B.只有②④ C.①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
“绿色化学”是21世纪化学发展的主导方向。“绿色化学”要求从根本上消灭污染,是一门能防止污染的科学。它包括“原料的绿色化”、“化学反应的绿色化”、“产物的绿色化”等内容。其中“化学反应的绿色化”要求反应物中所有的原子完全被利用且全部转入期望的产品中。下列不符合“化学反应的绿色化”的是( )
A.消除硫酸厂尾气中的SO2:SO2+2NH3+H2O= (NH4)2SO3
B.消除制硝酸工业尾气的氮氧化物:NO2+NO+2NaOH=2NaNO2+H2O
C.制CuSO4:Cu+2H2SO4(浓)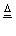 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D.制CuSO4:2Cu+O2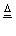 2CuO,CuO+H2SO4(稀)=CuSO4+H2O
2CuO,CuO+H2SO4(稀)=CuSO4+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
重水(D2O)是重要的核工业原料,下列说法错误的是
A.氘(D)原子核外有1个电子 B.1H与D互称同位素
C.H2O与D2O互称同素异形体 D.1H218O与D216O的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
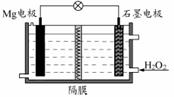
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是
A.Mg电极是该电池的正极 B.H2O2在石墨电极上发生氧化反应
C.石墨电极附近溶液的pH增大 D.溶液中Cl-向正极移动
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是
A.Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点
B.原子半径:Z>Y>X
C.CaY2与水发生氧化还原反应时,CaY2只作氧化剂
D.CaY2和CaZ22种化合物中,阳离子与阴离子个数比均为1︰2
查看答案和解析>>
科目:高中化学 来源: 题型:
甲烷是天然气的主要成分,是一种高效、低耗、污染小的清洁能源。下列
有关甲烷的说法正确的是 ( )
A、甲烷燃烧,火焰明亮,冒黑烟
B、物质的量1∶1的甲烷与氯气发生取代反应时,生成物只有CH3Cl和HCl
C、0.5mol甲烷完全燃烧时消耗氧气最多为1mol
D、甲烷分子中的所有原子均满足最外层8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,某水溶液中存在的离子有:Na+、B2-、HB-、H+、OH-,存在的分子有H2O、H2B。根据题意回答下列问题:
(1)写出酸H2B的电离方程式 ﹑ 。
(2)常温下,已知0.1 mol·L-1二元酸H2B溶液中c(OH-) / c(H+)=1×10-6。
①常温下,0.1 mol·L-1H2B溶液的pH= ;
②写出该酸(H2B)与少量NaOH溶液反应的离子方程式: ;
(3)t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw= 。该温度下(t℃),0.1 mol·L-1HCl溶液的pH= ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com