
����˵����ȷ����(����)
A��������һ��������ʵ���ҵ��������ʱ�����뾡�����ռ�����������
B����pH�ơ��絼����(һ�ֲ�����Һ��������������)���ɼ������������ˮ��̶�
C���ڱ���������ؿ����ڱ궨NaOH��Һ��Ũ�ȡ���������ڱ����������ʱ������ƽ������ʵ������ƫ�����õ�NaOH��ҺŨ�ȱ�ʵ��Ũ��ƫС
D����ij��Һ�м�������ͪ�Լ���������к���Һ��������ɫ������жϸ���Һ���е�����
B��[����] ����������������ռ���Ӧ����Ʒ�ʹ��ת��Ϊ��������ˮ��HgS��A��������������Ƿǵ���ʣ������ܵ��磬����ˮ����������ǵ����(����)����Һ�ܵ��磬B����ȷ�����������ڱ���������صĶ�����ʵ������ƫ��ʱ����������Ƶ��ڱ������������Һ��Ũ��ƫС���������ĵ��ڱ������������Һ�����ƫ�����õ�NaOH��ҺŨ�ȱ�ʵ��Ũ��ƫ��C��������ఱ����Ҳ��������ͪ������Ӧ������ɫ������D�����


 ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
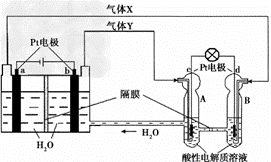
�ռ�ʵ���ҡ��칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ�أ�RFC����RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ�ŵ�ء���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ����
A������0.1 mol����ת��ʱ��a������ 0.56 L O2����״���£�
B�����װ���л�ѧ��ת��Ϊ���ܣ��Ҷ�װ���е���ת��Ϊ��ѧ��
C��d���Ϸ����ĵ缫��Ӧ�ǣ�O2 + 4H+ + 4e- 2H2O
D��c���Ͻ��л�ԭ��Ӧ���Ҷ�װ��B�е�H+����ͨ����Ĥ����A
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�±��ж�Ӧ��ϵ��ȷ����(����)
��������������������������������
| A | CH3CH3��Cl2 CH2===CH2��HCl�D��CH3CH2Cl | ��Ϊȡ����Ӧ |
| B | ����֬�õ����� �ɵ��۵õ������� | ��������ˮ�ⷴӦ |
| C | Cl2��2Br��===2Cl����Br2 Zn��Cu2��===Zn2����Cu | ��Ϊ���ʱ���ԭ���û���Ӧ |
| D | 2Na2O2��2H2O===4NaOH��O2�� Cl2��H2O===HCl��HClO | ��Ϊˮ����ԭ����������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ�鷽���У����ܴﵽʵ��Ŀ�ĵ���(����)
| ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
| A | ����CH3CH2Br��NaOH��Һ���Ƿ���ˮ�� | ��CH3CH2Br��NaOH��Һ���ȡ���ȴ��ȡ���ϲ�ˮ��Һ����ϡHNO3�ữ������AgNO3��Һ���۲��Ƿ��������ɫ���� |
| B | ����Fe(NO3)2�����Ƿ����������� | ��Fe(NO3)2��Ʒ����ϡH2SO4�μ�KSCN��Һ���۲���Һ�Ƿ��� |
| C | ��֤Br2��������ǿ��I2 | ��������ˮ����KI��Һ�У��ټ���CCl4�������ã��ɹ۲쵽�²�Һ�����ɫ |
| D | ��֤Fe(OH)3���ܽ��С��Mg(OH)2 | ��FeCl3��Һ����Mg(OH)2����Һ�У����ɹ۲쵽�����ɰ�ɫ��Ϊ���ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�о�С��Ϊ̽���������������������绯ѧ��ʴ���͵�Ӱ�����أ�����Ͼ��ȵ��������ۺ�̿��������ƿ�ײ�������ƿ��(��ͼ��ʾ)���ӽ�ͷ�ι��е��뼸�δ�����Һ��ͬʱ���������е�ѹǿ�仯��
(1)���������ʵ����Ʊ�(���в�Ҫ���ո�)��
| ��� | ʵ��Ŀ�� | ̿��/g | ����/g | ����/% |
| �� | Ϊ����ʵ�������� | 0.5 | 2.0 | 90.0 |
| �� | ����Ũ�ȵ�Ӱ�� | 0.5 | 36.0 | |
| �� | 0.2 | 2.0 | 90.0 |
������
(2)��Ţ�ʵ���������е�ѹǿ��ʱ��ı仯��ͼ(a)��ʾ��t2ʱ��������ѹǿ����С����ʼѹǿ����ԭ������������________��ʴ������ͼ(b)���ü�ͷ��������ø�ʴʱ���ӵ���������ʱ��̿�۱��淢����________(���������ԭ��)��Ӧ����缫��Ӧʽ��__________��
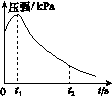 ������������
������������
������(a)������������������������(b)
(3)��С���ͼ(a)��0��t1ʱѹǿ����ԭ����������¼��裬������ɼ������
����һ���������ⸯʴ���������壻
�������________��
����
(4)Ϊ��֤����һ��ijͬѧ����˼����ռ����������Ƿ���H2�ķ��������������һ��ʵ�鷽����֤����һ��д��ʵ�鲽��ͽ��ۡ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���н����У�������Ȼ�γɵ��������ܱ����ڲ��������������������(����)A��K B��Na C��Fe D��Al
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����йؽ�����˵���в���ȷ����(����)
A�������������Ŀ���ʴ��ǿ
B����ͭ������֡�Ӳ�����ǺϽ�
C�����ڿ�������ʴ���������Dz����ý���
D������ȱ�ƻ������������֢��ȱ��������ƶѪ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�л���Ľṹ��ʽΪ �����й��ڸ��л������������ȷ����(����)
�����й��ڸ��л������������ȷ����(����)
A����������Ʒ�����Ӧ���ų�����
B�����ڴ�����������H2�����ӳɷ�Ӧ
C���ܷ���������Ӧ
D����ŨH2SO4�����������ᷢ��������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ⱦ�����Чȥ������Դ�ij�������ǻ�ѧ�츣�������Ҫ�о����⡣ij�о�С���������̿�(��Ҫ�ɷ�ΪMnO2��������������������ͭ�����Ƚ���������)���������ͨ�����¼����̼��ѳ�ȼúβ���е�SO2�����Ƶõ�ز���MnO2(��Ӧ������ʡ��)��
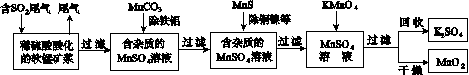
��ش��������⣺
(1)������������ʵ����____(ѡ��������ĸ���)��
A����������ۺ�����
B����ɫ��Ⱦ�ļ���
C������ļ���
(2)��MnCO3�ܳ�ȥ��Һ�е�Al3����Fe3������ԭ����________________________________��
(3)��֪��25 �桢101 kPaʱ��
Mn(s)��O2(g)===MnO2(s)����H����520 kJ/mol
S(s)��O2(g)===SO2(g)����H����297 kJ/mol
Mn(s)��S(s)��2O2(g)===MnSO4(s)��
��H����1065 kJ/mol
SO2��MnO2��Ӧ������ˮMnSO4���Ȼ�����ʽ��____________________________________��
(4)MnO2�����������������ϡ��ö��Ե缫���MnSO4��Һ���Ƶ�MnO2���������ĵ缫��Ӧʽ��________________________________��
(5)MnO2�Ǽ���п�̵�ص��������ϡ�����п�̵�طŵ�ʱ�������ĵ缫��Ӧʽ��________________��
(6)�����ѳ���SO2ֻ�����̿��е�MnO2��Ӧ������ͼʾ���̣���a m3(��״��)��SO2���������Ϊb%��β��ͨ�����SO2���ѳ���Ϊ89.6%�����յõ�MnO2������Ϊc kg�����ȥ��������ͭ����������ʱ�����������Ԫ���൱��MnO2________kg��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com