
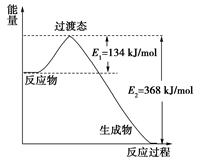
 2CH3OH(g) ΔH=+37 kJ·mol-1
2CH3OH(g) ΔH=+37 kJ·mol-1 3H2(g) + CO2(g) ΔH=+49 kJ·mol-1
3H2(g) + CO2(g) ΔH=+49 kJ·mol-1 CO(g) + H2O(g) ΔH=+41.3 kJ·mol-1
CO(g) + H2O(g) ΔH=+41.3 kJ·mol-1 度相同的3个密闭容器中,按不同方式
度相同的3个密闭容器中,按不同方式 投入反应物,保持恒温、恒压,发生反应①,测得反应达到平衡时的有关数据如下。
投入反应物,保持恒温、恒压,发生反应①,测得反应达到平衡时的有关数据如下。| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CH3OCH3、1mol H2O | 2mol CH3OH | 1mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 吸收a kJ | 放出b kJ | 放出c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α 1 | α 2 | α 3 |
 C. V1 > V3 D. c1=
C. V1 > V3 D. c1= 2c3
2c3 。
。科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.键能越大,表示该分子越容易受热分解 |
| B.共价键都具有方向性 |
| C.在分子中,两个成键的原子间的距离即为键长 |
| D.H—Cl的键能为431.8 k J /mol,H—Br的键能为366 k J /mol,这可以说明HCl分子比HBr分子稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 放出46.2 kJ的热量。则N—H键的键能是_______________________。
放出46.2 kJ的热量。则N—H键的键能是_______________________。 .5 kJ/mol ③
.5 kJ/mol ③ (g) △H= ― 393.5kJ/mol
(g) △H= ― 393.5kJ/mol )=2H2O(g) △H= ― 483.6kJ/mol
)=2H2O(g) △H= ― 483.6kJ/mol查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 列叙述中正确的是( )
列叙述中正确的是( )| A.MgSO4晶体中只存在离子键 |
| B.CH4、CO2都是由极性键构成的 |
| C.碱金属位于周期表中ⅠA主族,其密度均小于水 |
| D.次氯酸的结构式:H—Cl—O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲同学:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解吸热 |
B.乙同学:用加热的 方法可除去KNO3溶液中混有的Fe3+,说明含Fe3+的盐水解吸热 方法可除去KNO3溶液中混有的Fe3+,说明含Fe3+的盐水解吸热 |
| C.丙同学:通过实验发现同浓度的热的纯碱液比冷的纯碱液去油污效果好,说明碳酸钠水解吸热 |
| D.丁同学:在纯碱液中滴入酚酞试液,加热(不考虑水蒸发)后若红色加深,说明碳酸钠水解吸热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com