
向200mL Na2CO3和Na2SO4混合溶液中加入足量的BaCl2溶液,得到29.02g白色沉淀,用过量稀硝酸处理后剩余沉淀9.32g,并有气体产生。求:
(1)剩余沉淀的物质的量为___________ ;
(2)产生的气体在标准状况下的体积为___________ ;
(3)原混合溶液中Na+物质的量浓度为__________ _,Na2SO4的质量为___________ 。
计算过程:
【答案】
(1)0.04mol
(2) 2.24L
(3) c(Na+)=0.5mol/L, m(Na2SO4)=5.68g
【解析】BaSO4不溶于稀硝酸,BaCO3溶于稀硝酸。因此剩余的沉淀是BaSO4。
(1)n(BaSO4)=9.32g÷233g·mol-1=0.04mol
(2)n(CO2)=n(BaCO3)= (29.02g-9.32g) ÷233g·mol-1=0.1mol;
V(CO2)= 0.1mol×22.4L/mol=2.24L
(3)n(Na+)=2 n(Na2CO3)+ 2n(Na2SO4)=1mol;c(Na+)=0.5mol/L;
n(Na2SO4)= n(BaSO4)=0.04mol,即m(Na2SO4)=5.68g。


科目:高中化学 来源: 题型:
不能用胶体的知识解释的现象是
A. 向FeCl3溶液中加入NaOH溶液,出现红褐色沉淀
B. 一支钢笔使用两种不同牌号的墨水,易出现堵塞
C. 医疗上常用血液透析治疗由肾功能衰竭等疾病引起的尿毒症
D.江河入海处,易形成沙洲
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.298K,1.01×105Pa,64gSO2中含有的原子数为3NA
C. 11.2L Cl2含有的分子数为0.5NA
D.标准状况下,11.2LCCl4含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
有一包固体粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三种物质组成,取样品进行如下实验,从实验可以判断:

A.该固体粉末中一定不含有BaCl2
B.该固体粉末中一定含有KNO3
C.它的组成可能是CaCO3、BaCl2、CuSO4
D.它的组成一定是CaCO3、Na2SO4、KNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
依据元素周期律及元素周期表知识,下列推断正确的是 ( )。
A.酸性:H2SiO3>H2CO3
B.热稳定性:H2Se>H2S>H2O
C.碱性:CsOH>Ca(OH)2
D.若离子半径:R2->M+,则原子序数:R>M
查看答案和解析>>
科目:高中化学 来源: 题型:
化学键使得一百多种元素构成了世界的万物。关于化学键的下列叙述中,正确的是( )。
A.离子化合物中一定含有共价键,共价化合物中不含离子键
B.共价化合物中可能含离子键,离子化合物中只含离子键
C.构成单质分子的粒子一定含有 共价键
共价键
D.在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子、
原子核与原子核之间的排斥作用
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是  ( )。
( )。
A.两种微粒,若核外电子排布完 全相同,则其化学性质一定相同
全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.两原子如果核外电子排布相同,则一定属于同种元 素D.阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同
素D.阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)根据结构对有机物进行分类,有助于对其性质的掌握。
①下列有机物属于芳香烃的是 (填字母)。它与苯的关系是 ,写出苯与硝酸发生反应的化学方程式 ,预测该芳香烃 (填“能”或“不能”)发生该类反应。a.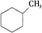 b.
b.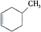 c.
c.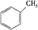
②下列有机物属于羧酸类的是 (填字母)。
a.CH3CHO b.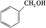 c.
c.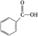
(2)化合物X的结构简式为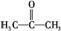
①X分子有 种氢原子。
②X的另一种同分异构体Z的结构简式为CH2=CH—CH2OH,请写出Z与Br2发生反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com