
| A. | O2与Cu反应生成CuO,S与Cu反应生成CuS | |
| B. | CaC2能水解:CaC2+2H2O=Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O═4Al(OH)3+3CH4↑ | |
| C. | 根据化合价Fe3O4可表示为FeO•Fe2O3,则Pb3O4也表示为PbO•Pb2O3 | |
| D. | SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液不产生沉淀 |
分析 A.硫单质的氧化性较弱和变价金属反应生成低价化合物;
B.盐的水解原理是:离子和氢离子或是氢氧根离子结合的过程;
C.四氧化三铅(Pb3O4)中铅的化合价为+2和+4价;
D.硝酸有强氧化性.
解答 解:A.硫单质的氧化性较弱,和变价金属反应生成低价化合物,则S与Cu反应生成Cu2S,而不能生成CuS,故A错误;
B.盐的水解原理是:离子和氢离子或是氢氧根离子结合的过程,Al4C3能水解,原理是铝离子和氢氧根离子结合,碳离子和氢离子结合,即Al4C3+12H2O═4Al(OH)3↓+3CH4↑,故B正确;
C.Pb在化合物里显+2价和+4价,根据化合价代数和为零的原则,Pb的+2价和+4价两种氧化物形式为PbO和PbO2,则Pb3O4的氧化物的表示形式可以写成 2PbO•PbO2,故C错误;
D.SO2通入Ba(NO3)2溶液中,亚硫酸电离生成氢离子,与硝酸根能氧化亚硫酸根为硫酸根,有白色沉淀,故D错误.
故选B.
点评 本题考查化学反应的基本原理,难度中等,明确反应原理是解题的关键,考查新信息获取、处理及灵活运用所学知识进行分析问题、解决问题的能力.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | (1)(4)(5) | B. | (2)(5) | C. | (1)(3) | D. | (2)(3)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2溶于水和H2SO3分解 | |
| B. | H2跟I2化合成HI和HI分解 | |
| C. | SO2跟O2化合成SO3和SO3分解 | |
| D. | NH3与HCl化合生成NH4Cl和NH4Cl受热分解生成NH3和HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
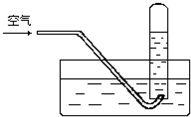
| A. | 若最终有气体剩余,气体呈红棕色 | B. | 若最终有气体剩余,气体是NO | ||
| C. | 试管内溶液为稀的硝酸溶液 | D. | 试管内的液面高度肯定会上升 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3→NaAlO2 | B. | Fe→FeCl3 | C. | Na2O→Na2CO3 | D. | SiO2→H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应中得失电子总数一定相等 | |
| B. | 有单质参加的反应一定是氧化还原反应 | |
| C. | 电解质溶液中阴阳离子的总数一定相等 | |
| D. | 分解反应一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
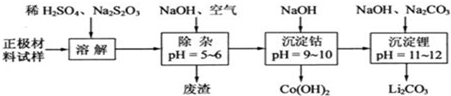
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:A2->D->B+ | |
| B. | 元素B、C的最高价氧化物对应水化物的碱性:B>C | |
| C. | 简单氢化物的稳定性:A>D | |
| D. | A与B形成的化合物中可能既有离子键又有共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com