
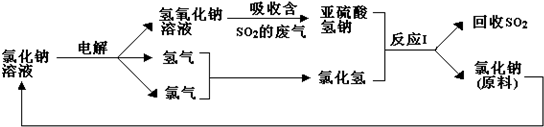
·ÖĪö £Ø1£©¶žŃõ»ÆĮņŌŚæÕĘųÖŠŗĶĖ®·“Ӧɜ³ÉČżŃõ»ÆĮņ£¬ČÜÓŚĖ®ŠĪ³ÉĮņĖį£¬ĖįÓź¶ŌÉśĪļÓŠ¼«“óµÄĪ£ŗ¦£»
£Ø2£©ĖįŠŌŃõ»ÆĪļŗĶ¼īŠŌŃõ»ÆĪļ·“Ӧɜ³ÉŃĒĮņĖįŃĪ£»ŃĒĮņĖįŃĪ²»ĪČ¶Ø£¬¼«Ņ×±»æÕĘųÖŠŃõĘųŃõ»ÆÉś³ÉĮņĖįŃĪ£»
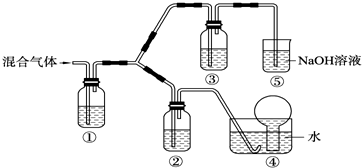
£Ø3£©¢Łøł¾ŻĶ¼ÖŖ£¬ÄÜŃ»·ĄūÓƵÄĪļÖŹŹĒĀČ»ÆÄĘ£»
¢ŚŃĒĮņĖįĒāÄĘŗĶĻ”ŃĪĖį·¢Éśø“·Ö½ā·“Ӧɜ³ÉĀČ»ÆÄĘ”¢¶žŃõ»ÆĮņŗĶĖ®£®
½ā“š ½ā£ŗ£Ø1£©ĖįÓźŹĒÓÉÓŚČĖĄą“óĮæŹ¹ÓĆĆŗ”¢ŹÆÓĶ”¢ĢģČ»ĘųµČ»ÆŹÆČ¼ĮĻ£¬Č¼ÉÕŗó²śÉśµÄĮņŃõ»ÆĪļ»ņµŖŃõ»ÆĪļ£¬ŌŚ“óĘųÖŠ¾¹żø“ŌӵĻÆѧ·“Ó¦ŗ󣬊Ī³ÉĮņĖį»ņĻõĖįĘųČܽŗ£¬»ņĪŖŌĘ”¢Óź”¢Ń©”¢Īķ²¶×½ĪüŹÕ£¬½µµ½µŲĆę³ÉĪŖĖįÓź£®ĖįÓźÖ±½ÓĪ£ŗ¦Ö²ĪļµÄŃæŗĶŅ¶£¬ŃĻÖŲŹ±Ź¹³ÉʬµÄÖ²ĪļĖĄĶö£®»¹æÉŅŌøÆŹ“½ØÖžĪļ¼°ĘäĖūĪļĘ·£®ĖįÓźĪ£ŗ¦Ė®ÉśÉśĪļ£¬ĖüŹ¹Šķ¶ąŗÓ”¢ŗžĖ®ÖŹĖį»Æ£¬µ¼ÖĀŠķ¶ą¶ŌĖįĆōøŠµÄĖ®ÉśÉśĪļÖÖČŗĆš¾ų£¬ŗž²“Ź§Č„ÉśĢ¬»śÄÜ£¬×īŗó±ä³ÉĖĄŗž£®ĖįÓź»¹É±ĖĄĖ®ÖŠµÄø”ÓĪÉśĪļ£¬ĘĘ»µĖ®ÉśÉśĢ¬ĻµĶ³“ĖĶā£¬Ėį»ÆµÄĖ®Ō“ĶžŠ²ČĖĆĒµÄ½”æµ£¬ĖįÓź¶ŌÉśĪļÓŠ¼«“óµÄĪ£ŗ¦£¬Ņņ“Ė±»³ĘĪŖ”°æÕÖŠĖĄÉń”±£¬
¹Ź“š°øĪŖ£ŗŠĪ³ÉĖįÓź£»
£Ø2£©¶žŃõ»ÆĮņŹĒĖįŠŌŃõ»ÆĪļ£¬¶žŃõ»ÆĮņŗĶCaO·“Ӧɜ³ÉŃĒĮņĖįøĘ£»ŃĒĮņĖįøĘ²»ĪČ¶Ø£¬¼«Ņ×±»æÕĘųÖŠŃõĘųŃõ»ÆÉś³ÉĮņĖįøĘ£¬·“Ó¦·½³ĢŹ½ĪŖCaO+SO2ØTCaSO3”¢2CaSO3+O2ØT2CaSO4£¬
¹Ź“š°øĪŖ£ŗĖįŠŌ£»
£Ø3£©¢Łøł¾ŻĶ¼ÖŖ£¬ÓĆĀČ»ÆÄĘČÜŅŗµē½āµĆµ½NaOH”¢ĀČĘų”¢ĒāĘų£¬ŃĒĮņĖįĒāÄĘŗĶĻ”ŃĪĖį·“Ӧɜ³ÉĀČ»ÆÄĘ£¬ŃĒĮņĖįÄĘÄÜŃ»·ĄūÓƵÄĪļÖŹŹĒĀČ»ÆÄĘ£¬
¹Ź“š°øĪŖ£ŗĀČ»ÆÄĘ£»
¢ŚŃĒĮņĖįĒāÄĘŗĶĻ”ŃĪĖį·¢Éśø“·Ö½ā·“Ӧɜ³ÉĀČ»ÆÄĘ”¢¶žŃõ»ÆĮņŗĶĖ®£¬Ąė×Ó·“Ó¦·½³ĢŹ½ĪŖHSO3-+H+=H2O+SO2”ü£¬
¹Ź“š°øĪŖ£ŗHSO3-+H+=H2O+SO2”ü£®
µćĘĄ ±¾Ģāæ¼²éĮņ¼°Ęä»ÆŗĻĪļŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬Ć÷Č·Į÷³ĢĶ¼ÖŠ·¢ÉśµÄ·“Ó¦ŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢Ņā£ŗŃĒĮņĖįŃĪ²»ĪČ¶Ø£¬¼«Ņ×±»Ńõ»Æ£¬ĪŖŅדķµć£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ£¬NaHCO3Čܽā¶Č±ČNa2CO3Š”£¬Ļņ±„ŗĶNa2CO3ČÜŅŗÖŠĶØČėCO2²śÉś³Įµķ | |
| B£® | ³£ĪĀ£¬SiO2ÓėĒā·śĖį”¢NaOHČÜŅŗ¾łæÉ·“Ó¦£¬SiO2ŹĒĮ½ŠŌŃõ»ÆĪļ | |
| C£® | BaSO3ÄŃČÜÓŚĖ®£¬SO2ĘųĢåĶØČėBa£ØNO3£©2ČÜŅŗÖŠ²śÉś³Įµķ | |
| D£® | ·Ē½šŹōŠŌ£ŗCl£¾S£¬ĖįŠŌ£ŗHClO£¾H2SO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚÖÜĘŚ±ķÖŠ£¬ŌŖĖŲµÄ×åŠņŹż¶¼µČÓŚĘäŌ×ÓµÄ×īĶā²ćµē×ÓŹż | |
| B£® | ÖÜĘŚ±ķÖŠ·Ē½šŹōŠŌ×īĒæµÄŌŖĖŲ£¬Ęä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĖįŠŌŅ²×īĒæ | |
| C£® | Ķ¬Ö÷×åŌŖĖŲĖęŌ×ÓŗĖµēŗÉŹżµÄµŻŌö£¬Ō×Ó°ė¾¶ŅĄ“ĪŌö“ó | |
| D£® | µŚ¢÷A×åŌŖĖŲµÄµ„ÖŹ£¬Ėę·Ö×ÓĮæµÄŌö“ó£¬ČŪ”¢·ŠµćÉżøߣ»¢ńA×åµ„ÖŹ£¬Ėę·Ö×ÓĮæµÄŌö“ó£¬ČŪ”¢·ŠµćÉżøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
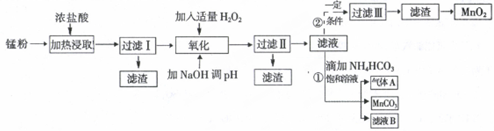
| ³ĮµķĪļ | Fe£ØOH£©2 | Fe£ØOH£©3 | Mn£ØOH£©2 | Zn£ØOH£©2 |
| ³ĮµķæŖŹ¼Ź±pH | 7.5 | 2.2 | 8.8 | 6.5 |
| ³ĮµķĶźČ«Ź±pH | 9.5 | 3.7 | 10.8 | 8.5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | CH3CH=CH2”” Ļ©Ģž 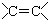 | B£® | 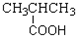 ōČĖį-COOH ōČĖį-COOH | ||
| C£® | 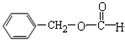 Č©Ąą”” Č©Ąą””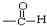 | D£® | RCH2OH £ØRĪŖĢž»ł£© “¼Ąą-OH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŌŖĖŲ | Al | B | Be | C | Cl | F | Li |
| µēøŗŠŌ | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| ŌŖĖŲ | Mg | N | Na | O | P | S | Si |
| µēøŗŠŌ | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ż¢Ž | B£® | ¢Ū¢Ü¢Ż¢Ž | C£® | ¢Ś¢Ü¢Ż¢Ž | D£® | ¢Ł¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | dcab | B£® | dabc | C£® | dbca | D£® | dbac |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com