
下列顺序不正确的是
| A.热稳定性:HF > HCl > HBr > HI |
| B.微粒的半径:Cl-> Na+> Mg2+> Al3+ |
| C.电离程度(同温度同浓度溶液中):HCl > CH3COOH > NaHCO3 |
| D.分散质粒子的直径:Fe(OH)3悬浊液 > Fe(OH)3胶体 > FeCl3溶液 |
 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:单选题
下列关于氢原子电子云图的说法正确的是
| A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大 |
| B.黑点密度大,单位体积内电子出现的机会大 |
| C.通常用小黑点来表示电子绕核作高速圆周运动 |
| D.电子云图是对电子运动无规律性的描述 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素A、B、C、D的原子序数依次增大。A原子的最外层电子数是内层电子数的2倍,元素B在同周期的主族元素中原子半径最大,元素C的合金是日常生活中常用的金属材料,D位于第VIA族。下列说法正确的是( )
A.原子半径:D>B>C>A
B.元素A、B的氧化物具有相同类型的化学键
C.元素B和C的最高价氧化物对应水化物的碱性:B>C
D.B、C、D的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质。已知:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1 mol/L 丁溶液的pH为13。下列说法正确的是( )
A.元素B在周期表中的位置为第二周期第VIA族
B.元素B、C、D的原子半径由大到小的顺序为r (D)>r(C)>r(B)
C.1.0 L、0. 1 mol/L戊溶液中阴离子总的物质的量小于0. 1 mol
D.1 mol甲与足量的乙完全反应共转移了约6.02×1023个电子
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关物质结构和性质的说法中,正确的是( )
| A.因为水溶液的酸性:HCl>H2S,所以非金属性:Cl>S |
| B.同周期第ⅡA族与第IIIA族的元素原子序数之差不一定为1 |
| C.元素原子的最外层电子数越多,越容易得电子,非金属性越强 |
| D.同周期主族元素的原子形成的简单离子电子层结构相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是
| A.Th 元素的质量数是232 | B.Th 元素的相对原子质量是231 |
| C.232Th 转换成233U是化学变化 | D.230Th和232Th的化学性质几乎相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是
| A.半导体材料砷化镓 | B.透明陶瓷材料硒化锌 |
| C.吸氢材料镧镍合金 | D.超导材料K3C60 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是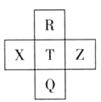
| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q |
| D.最高价氧化物的水化物的酸性: X > T |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
科学家用氘盐酸(DCl)和重水(D2O)溶液处理样品,对收集的气体加以分析,结果只发现有一些气体状态的碳氘化合物。这个实验不能用普通盐酸,其理由是( )
| A.普通盐酸的酸性太强 |
| B.普通盐酸具有挥发性 |
| C.普通盐酸和月球岩石中的碳化物无法反应 |
| D.无法区别岩石中原来含有的是含碳而不含普通氢的化合物,还是含碳和普通氢的化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com