


科目:高中化学 来源: 题型:
| A、石油裂解得到的汽油是纯净物 |
| B、石油产品都可用于聚合反应 |
| C、水煤气是通过煤的液化得到的气体燃料 |
| D、石油主要含有碳、氢两种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向KHSO4溶液中加入Ba(OH)2溶液至所得溶液呈中性Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、向Ca(HCO3)2溶液中滴入过量的NaOH溶液Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| C、钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| D、硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
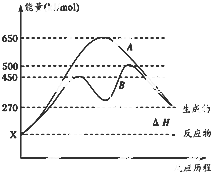 (1)已知:①Fe(s)+
(1)已知:①Fe(s)+| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
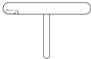 人们常用如右图所示仪器反复进行某物质的性质实验,如碘的升华实验.用该仪器能反复进行的还有:( )
人们常用如右图所示仪器反复进行某物质的性质实验,如碘的升华实验.用该仪器能反复进行的还有:( )| A、②④ | B、①③ | C、①④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
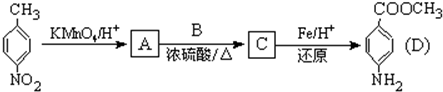
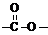 结构的基团的C的所有同分异构体的结构简式:
结构的基团的C的所有同分异构体的结构简式: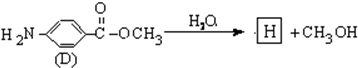
查看答案和解析>>
科目:高中化学 来源: 题型:
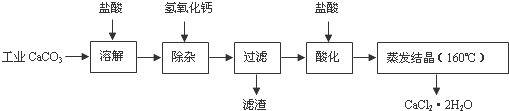
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com