
【题目】下列关于物质的量的叙述中,正确的是
A.1mol任何物质都含有6.02×1023个分子B.0.012gC-12中约含有6.02×1023个碳原子
C.1mol水中含有2mol氢和1mol氧D.1molH2分子中含有2molH
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
(1)请写出:D基态原子的价层电子排图:; F 基态原子的外围电子排布式: .
(2)下列说法错误的是 .
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点:SiO2>CO2 .
B.电负性顺序:B<C<D
C.N2与CO为等电子体,结构相似.
D.稳定性:H2O>H2S,水分子更稳定的原因是水分子间存在氢键.
(3)F离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点.向F的硫酸盐溶液中通入过量的C与A形成的气体X可生成(F(X)4)2+ , 该离子的结构式为(用元素符号表示).
(4)某化合物与F(Ⅰ)(Ⅰ表示化合价为+1)结合形成图1所示的离子,该离子中碳原子的杂化方式有 . 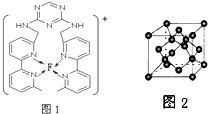
(5)B单质的一种同素异形体的晶胞如图2所示,则一个晶胞中所含B原子数为 .
(6)D与F形成离子个数比为1:1的化合物,晶胞与NaCl类似,设D离子的半径为a pm,F离子的半径b pm,求该晶胞的空间利用率 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组以H2O2的分解为例,研究浓度、催化剂、溶液的酸碱性对反应速率的影响。在常温下按照如下方案设计实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol/LFeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol/LFeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol/LFeCl3溶液 |
(1)实验①和②的目的是_________________________________。实验时由于没有观察到明显现象而无法得出结论。为了达到实验目的,你对原实验方案的改进措施是______________________________________________。
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图所示。
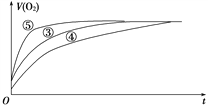
分析上图能够得出的实验结论是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得BeCl2为共价化合物,两个Be﹣Cl键间的夹角为180°,由此可判断BeCl2属于( )
A.由极性键形成的极性分子
B.由极性键形成的非极性分子
C.由非极性键形成的极性分子
D.由非极性键形成的非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气的制取及其性质的微型实验: ①用滤纸剪成四个适当大小的长方形,然后将这些滤纸都用凡士林粘在集气瓶内部。
②将饱和NaI、NaBr、Na2S、品红溶液(1~2滴)滴在如图所示的滤纸上。
③向集气瓶内加1.5 g KClO3 , 用滴管吸取约2 mL浓盐酸,然后将滴管装在双孔塞上,最后把该双孔塞塞在集气瓶上,如图所示。
④用滴管向漏斗中加NaOH溶液,注意所加NaOH溶液应以刚好装满漏斗下端的弯管处为宜(NaOH溶液在此起液封作用同时又有减压功能)
⑤挤压胶头滴管向集气瓶中加浓盐酸。
⑥整个现象看完后,用滴管向漏斗中加NaOH溶液吸收尾气。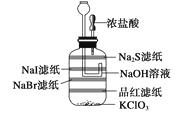
(1)该实验的主要现象: ;
(2)该实验的化学方程式:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究物质性质的基本程序是一个系统化的过程,其主干可分为四个步骤:
①观察物质的外观; ②实验和观察; ③解释和结论; ④预测物质的性质。
排列顺序正确的是
A. ②①④③ B. ①②③④ C. ①④②③ D. ④①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中,不会发生明显颜色变化的是
A. 氯化铜固体溶于水中 B. 硫酸铁溶液中滴加硫氰酸钾溶液
C. 氯化亚铁溶液中加入铜粉 D. 硫酸亚铁溶液中通入氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种胶体在电泳时,它的胶粒向阳极移动。在这胶体中分别加入下列物质:①乙醇溶液、②氯化钠溶液、③土壤、④氢氧化铁胶体,不会发生聚沉的是
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废旧黄铜(Cu、Zn合金,含少量杂质Fe)制备胆矾晶体(CuSO45H2O)及副产物ZnO.制备流程图如下: 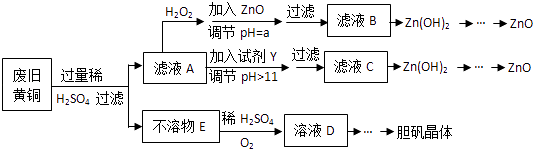
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2﹣下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0molL﹣1计算).
Fe3+ | Fe2+ | Zn2+ | |
开始沉淀的pH | 1.1 | 5.8 | 5.9 |
沉淀完全的pH | 3.0 | 8.8 | 8.9 |
请回答下列问题:
(1)加入ZnO调节pH=a的目的是 , a的范围是 .
(2)由不溶物E生成溶液D的化学方程式为 .
(3)滤液A中加入H2O2反应的离子方程式为 .
(4)由溶液D制胆矾晶体包含的主要操作步骤是 .
(5)下列试剂可作为Y试剂的是 . A.ZnO B.NaOH C.Na2CO3D.ZnSO4
若在滤液C中逐滴加入盐酸直到过量,则产生的现象是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com