
【题目】某学习小组利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去。)
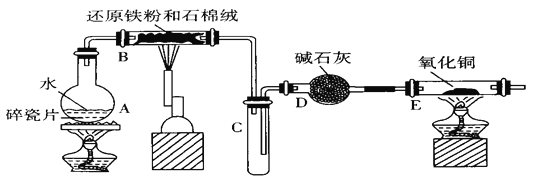
(1)装置B中发生反应的化学方程式是_____________________________________。
(2)装置E中的现象是_____________________________________。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤,简述检验滤液中Fe3+的操作方法:_____________________________________。
(4)该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
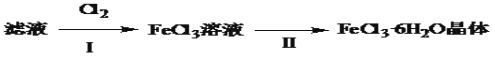
①步骤Ⅰ中通入Cl2发生反应的离子方程式______________________________。
②步骤Ⅱ从FeCl3稀溶液中得到FeCl3·6H2O晶体的主要操作包括:_________________。
【答案】3Fe+4H2O(g)![]() Fe3O4+4H2 黑色固体变红,右端管壁有水珠 取少量滤液,滴入几滴KSCN溶液,观察溶液是否出现血红色 Cl2+2Fe2+==2Cl-+2Fe3+ 加热浓缩,冷却结晶,过滤
Fe3O4+4H2 黑色固体变红,右端管壁有水珠 取少量滤液,滴入几滴KSCN溶液,观察溶液是否出现血红色 Cl2+2Fe2+==2Cl-+2Fe3+ 加热浓缩,冷却结晶,过滤
【解析】
根据物质性质书写化学方程式;根据实验原理及装置分析实验现象;根据铁离子的检验原理分析解答;根据溶液中溶质的性质分析物质分离提纯的操作方法。
(1)装置B中铁粉与水蒸气在高温下发生反应生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O(g)![]() Fe3O4+4H2,故答案为:3Fe+4H2O(g)
Fe3O4+4H2,故答案为:3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
(2)装置B铁与水蒸气反应生成的氢气,经碱石灰干燥后加入装置E,氧化铜与氢气加热发生反应生成了铜和水,所以反应的现象为:黑色的粉末变成紫红色,管壁产生水珠,故答案为:黑色的粉末变成紫红色,管壁产生水珠;
(3)用KSCN溶液检验滤液中Fe3+,观察溶液是否出现血红色,故答案为:取少量滤液,滴入几滴KSCN溶液,观察溶液是否出现血红色;
(4)①因为氯气具有强氧化性,所以能将二价铁离子氧化为三价铁离子,故答案为:Cl2+2Fe2+==2Cl-+2Fe3+
②由FeCl3稀溶液中得到FeCl36H2O晶体需加热浓缩、冷却结晶、过滤,故答案为:加热浓缩、冷却结晶、过滤。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法中正确的是
①20 g D2O含有的电子数为10NA
②含有1molFe(OH)3的氢氧化铁胶体中含有胶粒数为NA
③1 L0.1mol/L的NH4NO3溶液中氮原子数为0.2NA
④ 在标准状况下22.4 L SO3的物质的量为1mol
⑤25℃时,pH=12的l.0LNaClO溶液中水电离出的OH-的数目为0.01NA
⑥常温下,5.6 L NO和5.6 LO2的混合气体中含有的分子数为0.5NA
⑦l mol Na2O2与水完全反应时转移电子数为2NA
A. ③⑥⑦ B. ①③⑤ C. ①②④ D. ④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.标准状况下,22.4LCCl4含有的分子数为NA
B.常温常压下,64 g SO2含有的的原子数为3NA
C.78gNa2O2与水反应,转移电子个数为NA
D.配制物质的量浓度为0.5mol·L-1的MgCl2溶液,需MgCl2 47.5 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见元素A、B、M组成的四种物质发生反应:甲+乙=丙+丁,其中甲由A和M组成,乙由B和M组成,丙中只含有M。
(1)若甲为淡黄色固体,乙和丙均为常温下的无色无味气体。则甲中含有的化学键类型是___;常温下丁溶液显___性(填“酸”或“碱”或“中”),原因是____(用离子方程式表示);
(2)若丁为能使品红褪色的无色气体,丁与水反应生成戊,丙为常见红色金属,化合物甲、乙中原子个数比均为1∶2(M均显+1价),原子序数B大于A。回答下列问题:
①写出加热条件下上述生成丙的化学方程式____;
②已知常温下弱电解质的电离平衡常数如下:一水合氨![]() ,戊:
,戊:![]() ,
,![]() 。若一水合氨与丁恰好完全反应生成酸式盐,则浓度为
。若一水合氨与丁恰好完全反应生成酸式盐,则浓度为![]() 的该盐溶液pH___7(填“>”“<”或“=”);调整二者反应的比值可使溶液呈中性,此时溶液中
的该盐溶液pH___7(填“>”“<”或“=”);调整二者反应的比值可使溶液呈中性,此时溶液中![]() ____
____![]() (同上)。
(同上)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)=CH3OH(g)。在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应.测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。下列说法正确的是

A.该反应的△H<O,且p1<p2<p3
B.在C点时,H2转化率为75%
C.反应速率:v逆(状态A)>v逆(状态B)
D.在恒温恒压条件下,向该密闭容器中再充入1molCH3OH,
达平衡时CH3OH的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Zn、Ni,其均显+2价,下同),由铁酸盐MFe2O4经高温还原得到,常温下,它能使工业废气中的酸性氧化物分解除去,转化流程如下:

(1)已知铁酸盐(MFe2O4)被H2高温还原时,发生反应的MFe2O4与H2的物质的量之比为2∶1,则还原产物MFe2Ox中x=________,MFe2Ox中+2价铁与+3价铁的物质的量之比为_____。
(2)在酸性溶液中,Fe2O42-易转化为Fe2+:Fe2O42-+2e-+8H+=2Fe2++4H2O,有K2MnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种能使上述还原过程发生,写出该氧化还原反应的离子方程式并配平:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式中正确的是![]()
A.稀硝酸与过量的铁屑反应:![]()
B.硫酸铝溶液与过量的氨水反应:![]()
C.苯酚钠的水溶液中通入少量的![]() :
:![]()
D.醋酸钠的水解反应:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用氧化还原反应原理配平
(1)__NH3+___O2![]() ____NO +____H2O
____NO +____H2O
(2)____FeSO4+____KNO3+____H2SO4=____K2SO4+____Fe2(SO4)3+____NO↑+____H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1molNa2O2与SO2完全反应,转移2NA个电子
B. 标准状况下,11.2L乙醇中含有的极性共价键数目为3.5NA
C. 18g的D2O中含有的中子数为10NA
D. 1L0.1mol·L-1Fe2(SO4)3溶液中含有的阳离子数目小于0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com