
| A. | NA代表阿伏加德罗常数,1molC4H10中含共价键数目为14NA | |
| B. | 某反应的△H=-88kJ•mol-1,则正反应活化能一定小于88kJ•mol-1 | |
| C. | 已知某温度下,Kw=l×10-13,若将pH=8的NaOH溶液与pH=5的H2SO4溶液混合保持温度不变,欲使混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为11:9 | |
| D. | 将浓度为0.1 mol•L-1 HF溶液加水不断稀释过程中,电离度和Ka(HF)保持不变,$\frac{c({F}^{-})}{c({H}^{+})}$始终保持增大 |
分析 A、C4H10为丁烷,4个C原子有3个碳碳键;
B、焓变的大小决定于正逆反应的活化能的差值;
C、据Kw=l×10-13,Kw=c(OH-)×c(H+),PH=6.5时,溶液呈中性,pH=5的H2SO4溶液,c(H+)=1×10-5mol/L,pH=8的NaOH溶液,根据Kw=c(OH-)×c(H+),c(OH-)=$\frac{1×1{0}^{-13}}{1×1{0}^{-8}}$mol/L=1×10-5mol/L,要使混合液的pH=7,溶液呈碱性,即氢氧根离子过量,混合溶液中氢氧根离子的物质的量浓度=$\frac{1{0}^{-13}}{1{0}^{-7}}$=10-6 mol/L;
D、弱酸加水稀释,其电离度增大,电离平衡常数不变,氟离子和氢离子物质的量同等程度的增大.
解答 解:A、1molC4H10中含3个C-C、10个C-H共价键,则共价键数目为13NA,故A错误;
B、焓变的大小决定于正逆反应的活化能的差值,某反应的△H=-88kJ•mol-1,则正反应活化能不一定小于88kJ•mol-1,故B错误;
C、水的离子积常数为1×10-13,Kw=c(OH-)×c(H+),PH=6.5时,溶液呈中性,pH=5的H2SO4溶液,c(H+)=1×10-5mol/L,pH=8的NaOH溶液,根据Kw=c(OH-)×c(H+),c(OH-)=$\frac{1×1{0}^{-13}}{1×1{0}^{-8}}$mol/L=1×10-5mol/L,要使混合液的pH=7,溶液呈碱性,即氢氧根离子过量,混合溶液中氢氧根离子的物质的量浓度=$\frac{1{0}^{-13}}{1{0}^{-7}}$=10-6 mol/L,两种溶液混合后氢氧化钠的物质的量浓度为$\frac{1×1{0}^{-5}×Y-1×1{0}^{-4}×X}{X+Y}$=10-6mol/L,所以X:Y=11:9,故C正确;
D、将浓度为0.1 mol•L-1 HF溶液加水不断稀释过程中,电离度增大,Ka(HF)保持不变,$\frac{c({F}^{-})}{c({H}^{+})}$始终基本不变,故D错误;
故选C.
点评 本题考查了有机物中共价键的数目、焓变与活化能的关系、pH计算、弱酸稀释时电离度变化,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
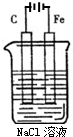 如图是电解NaCl溶液的示意图.请回答下列问题:
如图是电解NaCl溶液的示意图.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
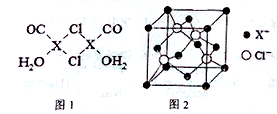 元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子,在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2•2CO•2H2O.
元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子,在气体分析中,常用XCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2XCl+2CO+2H2O═X2Cl2•2CO•2H2O.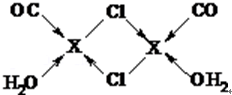 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②③④ | C. | ①②③ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,烷烃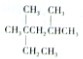 的名称是2,4-二甲基-2-乙基戊烷 的名称是2,4-二甲基-2-乙基戊烷 | |
| B. | 丙烯酸(CH2=CH-COOH)能发生取代加聚缩聚反应 | |
| C. | 糖类、油脂、蛋白质都是高分子化合物,一定条件下都能发生水解反应 | |
| D. | 等物质的量的HCOOCH3和CH3CHO完全燃烧,产物均通过足量的过氧化钠并充分反应,固体增重相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | iPhone5外壳易掉色原因是,铝壳表面氧化处理过程中作为阳极的金属铝纯度不够 | |
| B. | 道尔顿、汤姆生、卢瑟福、玻尔等科学家的研究不断更新人们对原子结构的认识 | |
| C. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 | |
| D. | 古代的陶瓷、砖瓦,现代的普通玻璃、水泥都是硅酸盐产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
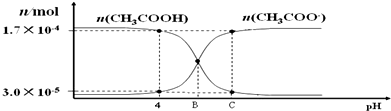
| A. | 醋酸的电离常数的表达式如下Ka=$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$ | |
| B. | pH=4 时,醋酸的电离常数 Ka≈1.8×10-5 | |
| C. | B点时的溶液中滴入酚酞溶液,显红色 | |
| D. | C点时,c(CH3COOˉ)>c(Na+)>c(H+)>c(OHˉ) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
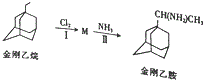 金刚乙烷、金刚乙胺等已经被批准用于临床治疗人感禽流感,且临床研究表明金刚乙烷比金刚乙胺的副作用小.
金刚乙烷、金刚乙胺等已经被批准用于临床治疗人感禽流感,且临床研究表明金刚乙烷比金刚乙胺的副作用小. ,如金刚乙烷表示为R-CH2CH3);
,如金刚乙烷表示为R-CH2CH3);
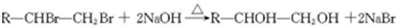 .
.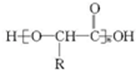 .
.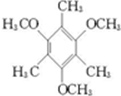 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com