
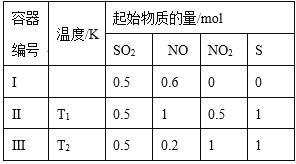
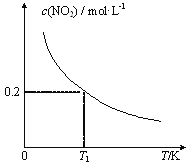
【题目】在3个体积均为1 L的恒容密闭容器中发生反应:SO2(g)+2NO(g)![]() 2NO2(g)+S(s)。改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是
2NO2(g)+S(s)。改变容器I的反应温度,平衡时c( NO2)与温度的关系如下图所示。下列说法正确的是
A. 该反应的ΔH<0
B. T1时,该反应的平衡常数为![]()
C. 容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比小于1:2
D. 若T2<T1,达到平衡时,容器Ⅲ中NO的体积分数小于40%
【答案】AD
【解析】A. 根据图像,升高温度,c( NO2)减小,说明平衡逆向移动,因此正反应为放热反应,ΔH<0,故A正确;B. T1时,平衡是c( NO2)=0.2 mol/L,
SO2(g)+2NO(g)![]() 2NO2(g)+S(s)
2NO2(g)+S(s)
起始(mol/L) 0.5 0.6 0 0
反应(mol/L) 0.1 0.2 0.2
平衡(mol/L) 0.4 0.4 0.2
该反应的平衡常数K=![]() =
=![]() ,故B错误;C. T1时,容器I平衡时气体的物质的量为0.4+0.4+0.2=1.0mol,容器Ⅱ中Qc=
,故B错误;C. T1时,容器I平衡时气体的物质的量为0.4+0.4+0.2=1.0mol,容器Ⅱ中Qc=![]() =0.5<
=0.5<![]() ,说明反应正向移动,气体的物质的量小于0.5+1+0.5=2.0mol,因此达到平衡,总压强之比大于1:2,故C错误;D.根据上述分析,T1时,平衡时容器I中NO的体积分数为
,说明反应正向移动,气体的物质的量小于0.5+1+0.5=2.0mol,因此达到平衡,总压强之比大于1:2,故C错误;D.根据上述分析,T1时,平衡时容器I中NO的体积分数为![]() ×100%=40%;容器I相当于起始时加入0.2mol二氧化氮和0.6mol二氧化氮,容器Ⅲ相当于起始时加入0.4mol二氧化硫和1.2mol一氧化氮,容器Ⅲ相当于容器I缩小体积的结果,根据方程式,增大压强,平衡正向移动,一氧化氮的物质的量减少,因此平衡时容器Ⅲ中NO的体积分数小于40%,若T2<T1,降低温度,平衡正向移动,一氧化氮的物质的量更少,故D正确;故选AD。
×100%=40%;容器I相当于起始时加入0.2mol二氧化氮和0.6mol二氧化氮,容器Ⅲ相当于起始时加入0.4mol二氧化硫和1.2mol一氧化氮,容器Ⅲ相当于容器I缩小体积的结果,根据方程式,增大压强,平衡正向移动,一氧化氮的物质的量减少,因此平衡时容器Ⅲ中NO的体积分数小于40%,若T2<T1,降低温度,平衡正向移动,一氧化氮的物质的量更少,故D正确;故选AD。


科目:高中化学 来源: 题型:
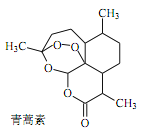
【题目】中医典籍《肘后备急方》所载治疗疟疾的方法“青蒿一握,以水二升渍,绞取汁,尽服之”, 对屠呦呦团队研发治疗疟疾的特效药——青蒿素有巨大的启示作用。屠呦呦在对比实验中发现古法疗效低下,她设计的提取青蒿素的工艺可以简化成如下流程:
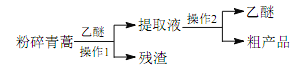
根据上述信息分析,下列判断或叙述中肯定错误的是
A. 从天然植物中提取有效成分治疗疾病是药物研发的重要途径
B. 将青蒿粉碎可以提高有效成分的提取率
C. 青蒿素易溶于水和乙醚
D. 操作 1 是过滤,操作 2 是蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:

(1)将标准状况下___L氯化氢气体通入1.00L水中可得36.5%的浓盐酸,该浓盐酸中HCl的物质的量浓度为___mol·L-1。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是_____。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol/L的稀盐酸。
①该学生需要量取___mL上述浓盐酸进行配制。
②配制仪器除烧杯、量筒和玻璃棒,还需要的仪器是___、____。
③配制时,下列操作正确的顺序是(用字母表示)____。
A.洗涤 B.定容 C.溶解 D.摇匀 E.冷却 F.称量 G.转移
④在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填“偏大”、“偏小”或“无影响”)。
Ⅰ.未等稀释后的溶液冷却到室温就转移到容量瓶(______)
Ⅱ.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水。(______)
Ⅲ.配制时,容量瓶有少量蒸馏水(______)
Ⅳ.定容时仰视刻度线。(_______)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是有机合成工业中应用较广泛的催化剂,见光易分解,在潮湿空气中易被氧化,难溶于水。
(1)实验室保存新制CuCl晶体的方法是_________________。
(2)已知:Cu(s)+Cl2(g)=CuCl2(s) △H1=-218.8kJ/mol
2Cu(s)+O2(g)=2CuO(s) △H2=-310.6kJ/mol
2CuCl2(s)=2CuCl(s)+Cl2(g) △H3=+152.3kJ/mol
则反应4CuCl(s)+O2(g)=2CuCl2(s)+2CuO(s)的△H=____kJ/mol。
(3)利用CuCl难溶于水的性质,可以除去废水中的Cl-。向含Cl-的废水中同时加入Cu和CuSO4,溶液中平衡时相关离子浓度关系如图所示。[已知:pc(离子)=-lgc(离子)]

①除去废水中Cl-的离子方程式为_________________。
②Ksp(CuCl)=___________。
③已知:Cu+Cu2+![]() 2Cu+ K=7.6×10-7。通过计算说明上述除Cl-的反应能完全进行的原因______________________________。
2Cu+ K=7.6×10-7。通过计算说明上述除Cl-的反应能完全进行的原因______________________________。
(4)T℃时,用H2还原CuCl制备活性铜:H2(g)+2CuCl(s)![]() 2Cu(s)+2HCl(g),达到平衡时,H2的转化率(
2Cu(s)+2HCl(g),达到平衡时,H2的转化率(![]() )为80%。反应速率v=v正-v逆=
)为80%。反应速率v=v正-v逆=![]() ,k正、k逆分别为正、逆反应速率常数,x为气体的物质的量分数。当
,k正、k逆分别为正、逆反应速率常数,x为气体的物质的量分数。当![]() =60%时,
=60%时,![]() =________(保留1位小数)。
=________(保留1位小数)。
(5)CuCl溶于浓氨水的反应原理为CuCl+2NH3·H2O![]() [Cu(NH3)2]-+2H2O+Cl-,该反应控制温度为70~80℃,其原因是_______________________。
[Cu(NH3)2]-+2H2O+Cl-,该反应控制温度为70~80℃,其原因是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为电解饱和食盐水的简易装置,下列有关说法正确的是:
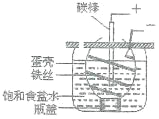
A. 电解一段时间后往蛋壳中滴加几滴酚酞,呈红色
B. 蛋壳表面缠绕铁丝是阳极
C. 铁丝表面生成的气体能使湿润的淀粉碘化钾试纸变蓝
D. 蛋壳可阻止生成的氯气与氢气、氢氧化钠溶液接触
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的有
①化学反应除了生成新物质外,还伴随着能量的变化
②放热反应不需要加热就能发生
③需要加热才能发生的反应都是吸热反应
④化学反应放热还是吸热。决定于生成物具有的总能量和反应物具有的总能量的大小
⑤热化学方程式应注明反应时的温度与压强,如没注明则表示常温常压时的反应
⑥等量的氢气和氧气分别完全燃烧生成气态水和液态水,前者放出的热量多
⑦H2(g)+I2(g) ![]() 2HI(g) ΔH=-QkJ·mol-1表示常温常压下,在恒温密闭容器中当有1mol H2和1mol I2(g)反应生成2 mol HI时放出QkJ的热量
2HI(g) ΔH=-QkJ·mol-1表示常温常压下,在恒温密闭容器中当有1mol H2和1mol I2(g)反应生成2 mol HI时放出QkJ的热量
⑧同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照条件下和点燃条件下的ΔH相同
A. 2项 B. 3项 C. 4项 D. 5项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。下列叙述中不正确的是:
A. 此时水的离子积Kw=1×10-14 B. 水电离出的c(H+)=1×10-10molL-1
C. 水的电离程度随温度升高而增大 D. c(Na+)=c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得25℃、101 kPa时,1 mol甲醇完全燃烧释放726.51kJ的热量,下列热化学方程式书写正确的是( )
A. 2CH3OH+3O2=2CO2+4H2O ΔH=-1453.02 kJ·mol-1
B. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=+1453.02 kJ·mol-1
C. CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-726.51 kJ·mol-1
D. CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-726.51 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以“火法粗炼”、“电解精炼”相结合的炼制精铜工艺流程如下,已知“还原”反应中,冰铜中的Cu2S先转化为Cu2O,然后Cu2O再与Cu2S反应生成粗铜。下列叙述正确的是
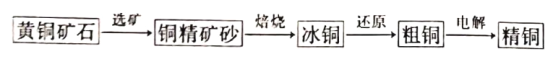
A. 该炼铜工艺对环境友好,不会产生大气污染物
B. “烙烧”过程中, CuFeS2既是氧化剂又是还原剂
C. 在Cu2S”还原”为Cu的总反应中,Cu2O作催化剂
D. “电解”时,金、银等贵金属被置换出来形成阳极泥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com