
【题目】通常情况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关叙述正确的是( )
A.分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B.分子中的所有原子均达到8电子稳定结构
C.NCl3分子是非极性分子
D.NBr3比NCl3易挥发
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
【题目】对于可逆反应4 NH3(g)+5O2(g)![]() 4NO(g)+6 H2O(g),下列叙述正确的是
4NO(g)+6 H2O(g),下列叙述正确的是
A. NH3和H2O化学反应速率关系是2v正(NH3)= 3v正(H2O)
B. 达到化学平衡时,4v正(O2)= 5v逆(NO )
C. 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D. 若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备溴乙烷的装置(已知溴乙烷的沸点38.4℃)。步骤如下:

①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在园底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热,使其充分反应。
已知:NaBr+H2SO4=HBr+NaHSO4
请回答下列问题:
(1)写出烧瓶中制备溴乙烷的化学方程式_______________________________________。
(2)溴乙烷的水溶性_____________(填“大于”“等于”或“小于”)乙醇的水溶性,其原因是_________________________________。
(3)反应时若温度过高,会有副反应发生,写出相应的化学方程式___________________________。(任写一个)
(4)反应结束后,U形管中粗制的溴乙烷呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的_________________(填序号)
A.H2O B.Na2SO3溶液 C.CCl4 D.NaOH溶液
除杂所需的主要玻璃仪器是______________(填仪器名称)。
(5)检验溴乙烷中溴元素:取少量溴乙烷,然后__________________(氨正确的操作顺序填序号)。
①加热; ②加入AgNO3溶液; ③加入稀HNO3酸化; ④冷却; ⑤加入NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间不能发生离子反应的是
A. Na2SO4溶液与BaCl2溶液 B. NaOH溶液和稀H2SO4溶液
C. NaCl溶液与KNO3溶液 D. Na2CO3溶液与稀盐酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是

选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
D | 液溴 | 苯 | 生成白雾 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环。
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气。下图表示恒压容器中0.5 mol CO2和1.5 mol H2转化率达80%时的能量变化示意图。

①写出该反应的热化学方程式: 。
②能判断该反应达到化学平衡状态的依据是 。
a.容器中压强不变 b.H2的体积分数不变
c.c(H2)=3c(CH3OH) d.容器中密度不变
e.2个C=O断裂的同时有6个H-H断裂。
(2)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.下图是通过人工光合作用制备HCOOH原理的示意图。根据要求回答问题:
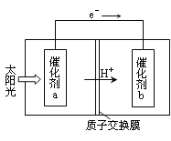
①该过程是将 转化为 。(以上两空选填“电能”“太阳能”“化学能”)
②催化剂b表面的电极反应方程式为 。
(3)某国科研人员提出了使用氢气和汽油(汽油化学式用C8H18表示)混合燃料的方案,以解决汽车CO2的排放问题。该方案主要利用储氢材料CaH2产生H2和用汽油箱贮存汽油供发动机使用,储氢系统又捕集汽油燃烧产生的CO2,该系统反应如下图所示:
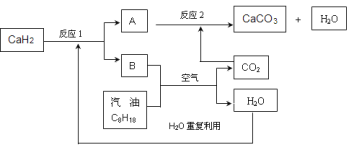
解决如下问题:
①写出CaH2的电子式 。
②反应1中氧化剂与还原剂的物质的量之比是: 。
③如该系统反应均进行完全,试写出该系统总反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石和石墨是碳元素的两种同素异形体.在100kPa时,1mol石墨转化为金刚石要吸收1.895kJ的热量,试判断在100kPa压强下,下列结论不正确的是
A. 石墨比金刚石稳定
B. 金刚石和石墨的微观结构不同
C. lmol石墨比lmol金刚石的总能量高
D. 石墨转化为金刚石是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是( )

A. 该装置将化学能转化为光能和电能
B. 该装置工作时,H+从b极区向a极区迁移
C. 每生成1mol O2,有44gCO2被还原
D. a电极的反应为:3CO2+18H+-18e-=C3H8O+5H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com