
【题目】下列元素的最高价正价和最低负价绝对值的差等于6的是
A.NB.SC.FD.Cl
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
【题目】氯化钠是日常生活的必需品,也是重要的化工原料。
(1)粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。

提供的试剂:
Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
①欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、_____________、_____________;
②用离子方程式表示加盐酸的作用是________________;_______________________;
(2)实验所得纯NaCl的质量大于粗盐中NaCl的质量,原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组拟提纯粗盐并取苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴,他们设计了如下流程:

请根据上述流程,回答以下问题:
(1)要从橙红色液体中分离出溴,可采取的操作是____________。
(2)试剂A中如果有两种溶质,它们是_____ 、 ______;如果是一种溶质,它是________。试剂B是__________。
(3)检验SO42- 已除尽的方法是__________________________________________。
(4)操作②名称_______________。
(5)在操作②之后的无色溶液中加入稀盐酸的目的是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu、Fe、Se、Co、S、P等元素常用于化工材料的合成。请回答下列问题:
(1)Fe3+最外层电子排布式为___________,其核外共有_____种不同运动状态的电子。Fe3+比Fe2+更稳定的原因是_______________________________________。
(2)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的电负性从大到小的顺序为_________________(用元素符号表示),SeO2分子的空间构型为___________________。
(3)P4S3可用于制造火柴,其分子结构如图所示。P4S3分子中硫原子的杂化轨道类型为__________,每个P4S3分子中含孤电子对的数目为_______________。

(4)铜的某种氧化物晶胞结构如图所示,若该晶胞的边长为a cm,则该氧化物的密度为________g·cm-3。(设阿伏加德罗常数的值为NA)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关说法正确的是( )
A. 46g乙醇中含有的共价键总数为7NA
B. FeBr2与等物质的量的Cl2充分反应时转移的电子数为3NA
C. 标准状况下,2.24LCHCl3中含有0.3NA个氯原子
D. 常温常压下,2.0g重水(D2O)中含有NA个中子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是
A.原子半径:Na>Si>ClB.还原性:Na>Mg>Al
C.稳定性:SiH4>H2S>HClD.酸性:H3PO4<H2SO4<HClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I是一种重要的有机化合物,其合成路线如图所示:
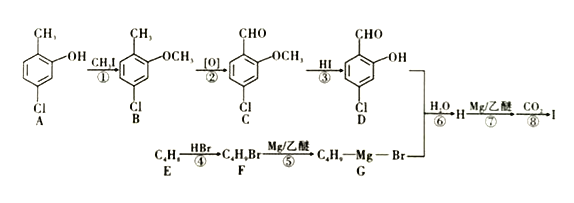
已知:
①有机物F结构中只有一种等效氢;
②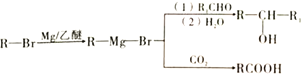
试根据相关知识回答下列问题:
(1)烃E的名称为_________,物质B含有的官能团的名称为________,B到C的反应类型是_________。
(2)在该过程中步骤①③两步设计的目的是_______________________,如果要检验合成的化合物B中是否含有A时,可用_______试剂。
(3)C能与新制的Cu(OH)2反应生成砖红色沉淀,试写出该反应的化学方程式:_____________________,化合物I的结构简式为_____________________________。
(4)芳香族化合物M(C8H7O2Br)能发生银镜反应,且苯环上只有两个取代基,满足上述条件的同分异构体一共有_______种。(提示:含有“-O-Br”结构的物质不稳定,不考虑)
(5)参照上述合成路线,以乙醇为基本原料(其他试剂自选),设计制备CH3CH2COOCH2CH3的合成路线。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)等质量的氧气和臭氧(O3),它们的物质的量之比为__________,所含分子数之比为__________,所含原子数之比为__________。
(2)中和含0.2molHCl的稀盐酸,需NaOH固体的质量为__________g。
(3)某气态氧化物的化学式为RO2,标准状况下1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为_____,R的相对原子质量为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com