
铅蓄电池的示意图如图所示。下列说法正确的是

A.放电时,N为负极,其电极反应式为: PbO2+SO42-+4H++2e-=PbSO4+2H2O
B.放电时,c(H2SO4)不变,两极的质量增加
C.充电时,阳极反应式为:PbSO4+2e-= Pb+SO42-
D.充电时,若N连电源正极,则该极生成PbO2
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源:2014-2015学年河南省高三12月月考理综化学试卷(解析版) 题型:填空题
(14分)某强酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32ˉ、SO42ˉ、SiO32ˉ、NO中的一种或几种离子,取该溶液进行实验,其现象及转化如下图。反应过程中有一种气体是红棕色。
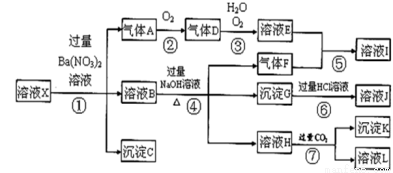
请回答下列问题:
(1)由强酸性条件即可判断溶液X中一定不存在的离子有 ;
(2)溶液X中,关于NO3-的判断一定正确的是 ;
A 一定有 B.一定没有 C.可能有
(3)产生气体A的离子方程式为 ;
(4)转化⑥发生反应的现象为 ;
(5)转化④中产生H的离子方程式为 ;
(6)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,则反应中D与O2的物质的量之比为 ;
(7)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液①NaOH溶液 ②KSCN溶液 ③石蕊试剂 ④pH试纸 ⑤KMnO4溶液 ⑥氯水和KSCN的混合溶液中的一种,根据现象即可判断,该试剂最好是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
向FeCl3、CuCl2的混合溶液中加入铁粉,充分反应仍有固体存在,则下列判断不正确的是
A.加入KSCN溶液一定不变红色 B.溶液中一定含Fe2+
C.溶液中一定含Cu2+ D.剩余固体中一定含Cu
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
有机物A、B、C、D、E、F、G、H相互转化关系如下图所示。5.2 g F能与100 mL 1 mol/L NaOH溶液恰好完全中和,0.1 mol F还能与足量NaHCO3反应,在标准状况下放出4.48 L CO2。D的分子式为C3H3O2Na,E的分子中含有羧基。
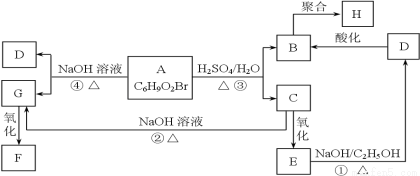
(1)写出物质C中的官能团的名称: ;
(2)写出物质F、H的结构简式;
F 、H ;
(3)写出反应①、④的化学反应类型:① 、④ ;
(4)写出变化①的化学方程式
(5)写出相对分子质量比B大14,且与B具有相同官能团的物质的结构简式(仅写一种)。
。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:选择题
有关下图所示原电池的叙述不正确的是
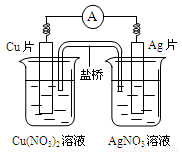
A.电子沿导线由Cu片流向Ag片
B.正极的电极反应是Ag++e-=Ag
C.Cu片上发生氧化反应,Ag片上发生还原反应
D.反应时盐桥中的阳离子移向Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、R的化合价与原子序数的关系如图所示

下列说法不正确的是
A.原子半径:Z>W>Y
B.Z和Y形成的化合物是离子化合物
C.气态氢化物的稳定性:R<Y
D.常温下单质W能溶于R的最高价氧化物对应水化物的浓溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:选择题
酸性溶液中粒子还原性顺序为Cl-<Fe2+<H2O2<I-<SO2,则下列反应中不能实现的是
A.2Fe3++SO2+2H2O =2Fe2++SO42-+4H+ B.I2+SO2+2H2O =H2SO4+2HI
C.H2O2+H2SO4 =SO2+O2+2H2O D.2Fe3++2I- =2Fe2++I2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高一上学期期中考试化学试卷(解析版) 题型:计算题
(6分)计算题:
(1)实验室用0.2L 0.5mol/L氢氧化钠溶液来吸收氯气尾气,并利用以下所给的方程式计算: 标准状况下,最多能吸收到多少升氯气?2NaOH+Cl2===NaCl+NaClO+H2O
(2)实验室配制0.5 mol·L-1硫酸溶液500 mL,需要质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为 mL。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
苯分子中的碳碳键不是单双键交替的,不能作出这种判断的证据是
A.苯的邻位二元取代物只有一种 B.苯环中碳碳键均相同
C.苯的一元取代物无同分异构体 D.苯不使酸性KMnO4溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com