
| A. | 葡萄糖能发生水解反应生成乙醇和二氧化碳 | |
| B. | 氨基乙酸、氯乙烯、乙二醇均可发生聚合反应 | |
| C. | 实验室用溴乙烷在浓硫酸、170℃条件下制备乙烯 | |
| D. | 苯酚能跟碳酸钠溶液反应,苯酚的酸性比碳酸强 |
分析 A.葡萄糖不能发生水解;
B.氨基乙酸中含有氨基和羧基,乙二醇中含有羟基,均可与一些物质反应脱去H2O,氯乙烯含有碳碳双键,可发生加聚反应;
C.溴乙烷在氢氧化钠、乙醇溶液中发生消去反应;
D.苯酚的酸性比碳酸弱.
解答 解:A.葡萄糖为单糖,不能发生水解,而在酒曲酶的作用下反应生成乙醇,故A错误;
B.氨基乙酸中含有氨基和羧基,乙二醇中含有羟基,均可与一些物质反应脱去H2O,氯乙烯含有碳碳双键,可发生加聚反应,故B正确;
C.乙醇在浓硫酸、170℃条件下制备乙烯,而溴乙烷在氢氧化钠、乙醇溶液中发生消去反应,故C错误;
D.苯酚的酸性比碳酸弱,苯酚能跟碳酸钠溶液反应生成碳酸氢钠和苯酚钠,故D错误.
故选B.
点评 本题考查了有机物的结构和化学性质、有机反应类型、化学实验方案的评价,为高频考点,涉及葡萄糖、苯酚、溴乙烷等物质的性质、消去反应的条件、乙烯的制备等,把握反应原理及反应条件为解答的关键,侧重有机物性质的考查,题目难度不大.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 含有大量AlO2-的溶液中:Na+、K+、HCO3-、NO3- | |
| B. | 中性溶液中:K+、Cl-、SO42-、Al3+ | |
| C. | 加Al粉产生H2溶液中:SO42-、K+、Cu2+、Cl- | |
| D. | pH=1的溶液中:NH4+、Na+、Fe3+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
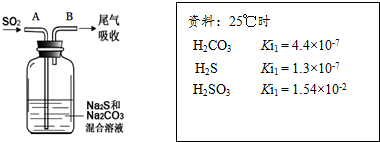
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应一定有单质参与 | |
| B. | 氧化还原反应的实质是电子转移 | |
| C. | 有元素化合价升降的反应一定是氧化还原反应 | |
| D. | 氧化剂在反应中化合价降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O和H2O+互为同分异构体 | B. | H2O+有较强的氧化性 | ||
| C. | 水分子形成的“网”是一种新化合物 | D. | H2O(s)→H2O(l)→H2O(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
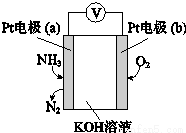
| A. | b极为负极 | |
| B. | a极的电极反应式为2NH3+3O2--6e-═N2+3H2O | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | 该传感器在工作过程中KOH的物质的量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
温度为T时,向 2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g) 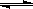 PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t / s | 0 | 50 | 150 | 250 | 350 |
n | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前50s的平均速率v(PCl3)=0.0032mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com