
【题目】【无机工业流程】

实验室从含碘废液(除H2O外,含有CCl4、I2、I- 等)中回收碘,其实验过程如下:
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程为 ;该操作将I2还原为I- 的目的是 。
(2)操作X的名称为____________。

(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40 ℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是 ;锥形瓶里盛放的溶液为 。
(4)已知:5SO![]() +2IO
+2IO![]() +2H+===I2+5SO
+2H+===I2+5SO![]() +H2O,某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO
+H2O,某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO![]() 中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO
中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO![]() 的实验方案:取适量含碘废水用CCl4多次萃取、分液直到水层用淀粉溶液检验不出有碘单质存在;____________________
的实验方案:取适量含碘废水用CCl4多次萃取、分液直到水层用淀粉溶液检验不出有碘单质存在;____________________
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液。
【答案】(1)SO32-+I2+H2O=2I-+SO42-+2H+,使四氯化碳中碘进入水层
(2)分液(3)使氯气在溶液中有较大的溶解度 氢氧化钠溶液
(4)从水层取少量的溶液,加入1—2mL淀粉溶液,加热盐酸酸化,滴加氯化铁溶液,若溶液变蓝,说明废水中含有碘离子;若溶液不变蓝,说明废水中不含有碘离子。另从水层取少量溶液,加入1—2mL淀粉溶液,加热盐酸酸化,滴加亚硫酸钠溶液,若溶液变蓝,说明废水中含有碘酸根离子,否则不含有。
【解析】试题分析:(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,亚硫酸根离子被氧化为硫酸根离子,离子方程式为SO32-+I2+H2O=2I-+SO42-+2H+;碘易溶于有机溶剂,碘离子易溶与水,所以把碘单质转化为碘离子的目的是使四氯化碳中碘进入水层。
(2)四氯化碳不溶于水,所以溶液分层,则用分液的方法除去四氯化碳。
(3)气体的溶解度随温度升高而降低,低温使氯气在溶液中有较大的溶解度;氯气有毒会污染空气,应用碱溶液吸收,即锥形瓶里盛放的溶液为NaOH溶液。
(4)需要检验碘离子和碘酸根离子,两种离子均应转化为碘单质用淀粉检验,前者需氧化剂,后者需还原剂,根据题意,具体操作为从水层取少量的溶液,加入1—2mL淀粉溶液,加热盐酸酸化,滴加氯化铁溶液,若溶液变蓝,说明废水中含有碘离子;若溶液不变蓝,说明废水中不含有碘离子。另从水层取少量溶液,加入1—2mL淀粉溶液,加热盐酸酸化,滴加亚硫酸钠溶液,若溶液变蓝,说明废水中含有碘酸根离子,否则不含有。


科目:高中化学 来源: 题型:
【题目】(1)下列各组物质:
A.金刚石与石墨;
B.淀粉与纤维素;
C.氕与氘;
D.甲烷与戊烷;
E.葡萄糖与果糖
F.![]() 与
与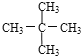
G.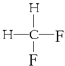 与
与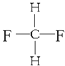
其中互为同位素 ;(填编号.下同),互为同系物的是 ,互为同分异构体的是 ,是同一种物质的是 .
(2)120℃,101kpa下,9ml由CO和C2H4组成的混合气体在足量的O2中完全燃烧后,恢复到原温度和压强.测得混合气体完全燃烧所消耗O2的体积与生成CO2的体积相等.请回答下列问题。
①等体积的CO和C2H4在相同条件下完全燃烧,生成CO2的体积比为 ;消耗O2的体积比为 .
②燃烧前混合气体中CO的体积为 , C2H4的体积为 .
(3)①化合物A的结构简式为: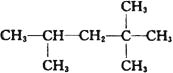 ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_______________;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为__________________。
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_______________;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为__________________。
②篮烷分子的键线式如图所示,试回答:
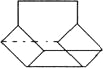
I写出篮烷分子的化学式____________;II篮烷分子的一氯取代物的种数为_______种。
(4)元素氮的一种液态氢化物叫肼,其分子中氮原子与氢原子个数比为1:2.肼﹣空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%﹣30%的KOH溶液.氮元素对应的燃烧产物为N2。该燃料电池的负极的电极反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.氯气通入氯化亚铁溶液中:Cl2+Fe2+=2Cl-+Fe3+
B.钠投入水中:Na+H2O=H2↑+Na++OH-
C.漂白粉的漂白原理:2ClO-+CO2+H2O=CO32-+2HClO
D.用小苏打治疗胃酸过多:HCO3-+H+=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W代表短周期的四种元素,有关它们的部分信息如下表所示:
元素 | 部分结构特点 | 部分性质 |
X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2等 |
Y | Y原子的次外层电子数等于最外层电子数的一半 | Y元素能形成多种单质 |
Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价的代数和等于6 |
W | 第三周期元素的简单离子中半径最小 | W的单质化学性质虽较活泼,但只需常温保存 |
请按要求回答下列问题(注意不能用字母X、Y、Z、W作答,请用相应的元素符号或化学式填写):
(1)X的元素名称是 ,X的气态氢化物的电子式是 。
(2)Z元素在周期表中的位置是第 周期,第 族。Z和W形成的化合物属于 化合物(填“离子”或“共价”)。
(3)X、Y、Z、W的原子半径从大到小的顺序是 。
(4)X、Y、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是: 。
(5)铜和X的最高价氧化物的水化物的浓溶液反应的化学方程式: 。
(6)气体分子(YX)2称为拟卤素,性质与卤素类似,请写出(YX)2与NaOH溶液反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 甲烷中混有少量乙烯,可将混合气体通入盛有酸性高锰酸钾溶液的洗气瓶中除去
B. 在苯中加入酸性KMnO4溶液,振荡并静置后下层液体为紫色
C. 在苯中加入溴的四氯化碳溶液,振荡并静置后下层液体为无色
D. 食物中含有大量的纤维素,可以在人体内直接水解成葡萄糖成为营养物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A.2:3 B. 1:5 C.1:4 D.2:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质发生变化时,所克服的粒子间相互作用完全相同的是( )
A.液态HF与液态HBr分别受热变为气体
B.氯化铵与苯分别受热变为气体
C.氯化钠与氯化氢分别溶解在水中
D.碘与干冰分别受热变为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化亚铜(CuH)是一种不稳定的物质,能在氯气中燃烧,也能与酸反应。用CuSO4溶液和“某物质”在40~50℃时反应可生成CuH。下列叙述中错误的是( )
A. “某物质”具有还原性
B. CuH与盐酸反应可能产生H2
C. CuH与足量稀硝酸反应:CuH+3H++NO3-=Cu2++NO↑+2H2O
D. CuH在氯气中燃烧:CuH+Cl2=CuCl+HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com