
 ����ϡ���ᡢ���������̼��ͭƬ��ʳ�Ρ���ʯ�ҡ���Ƭ��ľ̿��8�����ʣ�
����ϡ���ᡢ���������̼��ͭƬ��ʳ�Ρ���ʯ�ҡ���Ƭ��ľ̿��8�����ʣ����� ��1���������ˮ��Һ�л�����״̬���ܵ���Ļ����
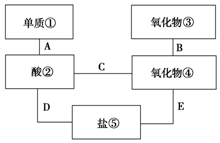
��2������Ŀ�ṩ�������У����ʢ�����ڷ�Ӧ�����ΪFe����ΪH2SO4���������ݷ�Ӧ�����ΪNa2CO3�������������ݷ�Ӧ�����ΪCaO�����������������������ܷ�Ӧ�����ΪCO2���ݴ˽��
��� �⣺��1��ϡ�����ǻ����Ȳ��ǵ����Ҳ���Ƿǵ���ʣ��������ڵ���ʣ�������̼�Ƿǵ���ʣ�ͭƬ�ǽ������ʣ��Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�ʳ���ǵ���ʣ���ʯ��Ϊ����ʣ���Ƭ�ǽ������ʣ��Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�ľ̿���ǵ��ʣ��Ȳ��ǵ����Ҳ���Ƿǵ���ʣ������������������ڵ���ʵ���Na2CO3��NaCl��CaO���ʴ�Ϊ��Na2CO3��NaCl��CaO��
��2��������Ŀ�ṩ�������У����ʢ�����ڷ�Ӧ�����ΪFe����ΪH2SO4���������ݷ�Ӧ�����ΪNa2CO3�������������ݷ�Ӧ�����ΪCaO�����������������������ܷ�Ӧ�����ΪCO2��
�ʴ�Ϊ��Fe��H2SO4��CO2��CaO��Na2CO3��
��A���ٺ͢ڷ�Ӧ�Ļ�ѧ����ʽ��Fe+H2SO4=FeSO4+H2����
B���ۺܷ͢�Ӧ�Ļ�ѧ����ʽ��CaO+CO2=CaCO3��
C���ںܷ͢�Ӧ�Ļ�ѧ����ʽ��H2SO4+CaO=CaSO4+H2O��
D���ں͢ݷ�Ӧ�Ļ�ѧ����ʽ��H2SO4+Na2CO3=Na2SO4+CO2��+H2O��
E���ܺ͢ݷ�Ӧ�Ļ�ѧ����ʽ��CaO+Na2CO3+H2O=CaCO3��+2NaOH��
�����л��ϼ۱仯ֻ��A1������ӦA�����ӷ���ʽΪFe+2H+�TFe2++H2������ӦBû�����Ӳ��룬���Բ��������ӷ�Ӧ����ӦD�Ļ�ѧ����ʽΪH2SO4+Na2CO3�TNa2SO4+H2O+CO2����
�ʴ�Ϊ��1��Fe+2H+�TFe2++H2���������ڣ�H2SO4+Na2CO3�TNa2SO4+H2O+CO2����
���� ���⿼�����ʵ��ж��Լ�������ƶϣ������ڻ���֪ʶ�Ŀ��飬�ѶȲ������ṩ���ʵ������Լ�ת����ϵ�����жϣ�


 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
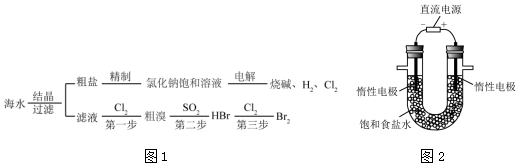
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 | B�� | 2 | C�� | 3 | D�� | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
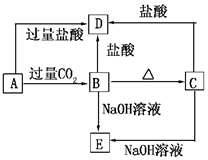 A��B��C��D��E���ֻ����������ij�ֳ���Ԫ�أ����ǵ�ת����ϵ��ͼ��ʾ������AΪ������Һ��CΪ���ܵİ�ɫ���壬E��������ˮ����ȡA��Һ���գ���ɫ��ӦΪdz��ɫ������ɫ�ܲ�������
A��B��C��D��E���ֻ����������ij�ֳ���Ԫ�أ����ǵ�ת����ϵ��ͼ��ʾ������AΪ������Һ��CΪ���ܵİ�ɫ���壬E��������ˮ����ȡA��Һ���գ���ɫ��ӦΪdz��ɫ������ɫ�ܲ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1��2 | B�� | 1��4��1 | C�� | 4��4��1 | D�� | 4��2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
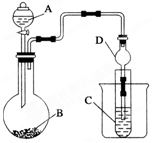 Ϊ̽��Ԫ�صķǽ����Եı仯���ɣ�ij��ѧ��ȤС��ͬѧ���������һϵ��ʵ�飬������ͼ��ʾװ�ã�
Ϊ̽��Ԫ�صķǽ����Եı仯���ɣ�ij��ѧ��ȤС��ͬѧ���������һϵ��ʵ�飬������ͼ��ʾװ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
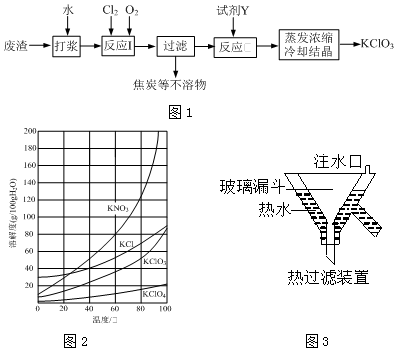
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư�ۡ�Cl2����ˮ��NaHCO3 | B�� | �������֡�����Cu2��OH��2CO3������ | ||
| C�� | ���ᡢSO2�����NH4Cl | D�� | ʳ�ס�C2H5OH�����Լء�NaHSO4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com