

| A. | 该燃料电池负极发生的电极反应为:N2H4+4OH--4e-═N2↑+4H2O | |
| B. | 用该燃料电池作为装置②的直流电源,产生7.1g Cl2至少需加入0.5 mol N2H4 | |
| C. | 该燃料电池中,电子从左侧电极经外电路流向右侧电极,溶液OH-迁移到左侧 | |
| D. | 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 |
分析 该燃料电池中,负极上燃料失电子发生氧化反应,左侧为负极,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O,正极上氧气得电子发生还原反应,右侧为正极,电极反应式为:O2+2H2O+4e-=4OH-,电池总反应为:N2H4+O2=N2↑+2H2O,根据串联电路中电子守恒计算,结合离子的移动方向、电流的方向分析解答.
解答 解:A.通入燃料的电极为负极,负极上燃料失电子发生氧化反应,电极反应式为:N2H4+4OH--4e-=N2↑+4H2O,故A正确;
B.电解氯化铜生成氯气的电极反应式为2Cl--2e-=Cl2↑,生成1mol氯气转移2mol电子,产生7.1g Cl2为0.1mol,燃料电池中的负极反应为:N2H4+4OH--4e-=N2↑+4H2O,则转移0.2mol电子,消耗0.05mol的N2H4,故B错误;
C.该燃料电池中,负极上燃料失电子发生氧化反应,左侧为负极,电子从左侧电极经外电路流向右侧电极,原电池中阴离子移向负极,所以溶液OH-迁移到左侧,故C正确;
D.因为电池中正负极上为气体参与的反应,所以采用多孔导电材料,可以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触,故D正确;
故选B.
点评 本题考查了燃料电池,明确正负极上发生的反应是解本题关键,难点是电极反应式的书写,要结合电解质溶液的酸碱性书写,注意原电池中阴离子移向负极,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 稀豆浆、硅酸、氯化铁溶液都属于胶体 | |
| B. | Na2O、MgO、Al2O3均属于碱性氧化物 | |
| C. | 氨水、次氯酸都属于弱电解质 | |
| D. | 葡萄糖、油脂都不属于有机高分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
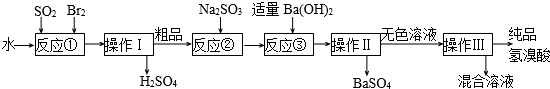
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
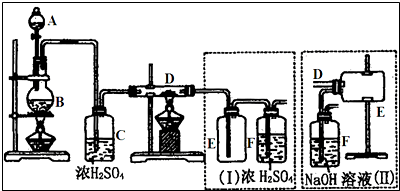
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | Na2O2 溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| C. | 大理石溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
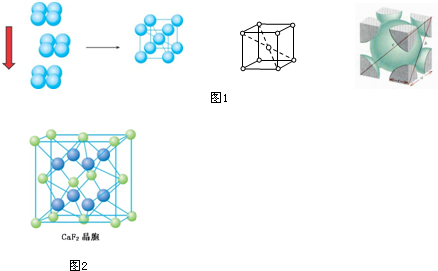
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.72L | B. | 24.4L | C. | 10.08L | D. | 13.44L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com