
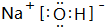 .
.分析 (1)元素甲是第3周期ⅦA族元素,则甲为Cl,甲元素与另两种非金属元素可组成离子化合物A,应是铵盐,即A为氯化铵,含有离子键与共价键;
(2)在第3周期元素的原子半径中(0族除外),元素乙的原子半径最大,则乙为Na,其最高价氧化物对应水化物为NaOH,由钠离子与氢氧根离子构成;
(3)金属元素丙形成的某化合物的溶液常用于检验CO2,则丙为Ca,电子层结构相同的离子,核电荷数越大离子半径越小;
元素丁的原子序数比丙小8,则丁为Mg,Mg在CO2中燃烧生成MgO与碳;
(4)元素戊是第3周期中简单离子半径最小的元素,则戊为Al,该元素的最高价氧化物对应水化物为氢氧化铝,与氢氧化钠反应生成偏铝酸钠与水.
解答 解:(1)元素甲是第3周期ⅦA族元素,则甲为Cl,甲元素与另两种非金属元素可组成离子化合物A,应是铵盐,即A为NH4Cl,含有离子键与共价键,故答案为:NH4Cl;离子键、共价键;
(2)在第3周期元素的原子半径中(0族除外),元素乙的原子半径最大,则乙为Na,其最高价氧化物对应水化物为NaOH,由钠离子与氢氧根离子构成,电子式为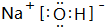 ,故答案为:
,故答案为: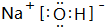 ;
;
(3)金属元素丙形成的某化合物的溶液常用于检验CO2,则丙为Ca,电子层结构相同的离子,核电荷数越大离子半径越小,故离子半径:r(Cl-)>r(Ca2+);
元素丁的原子序数比丙小8,则丁为Mg,Mg在CO2中燃烧生成MgO与碳,反应方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
故答案为:r(Cl-)>r(Ca2+);2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(4)元素戊是第3周期中简单离子半径最小的元素,则戊为Al,该元素的最高价氧化物对应水化物为氢氧化铝,与氢氧化钠反应生成偏铝酸钠与水,反应离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,
故答案为:Al(OH)3+OH-═AlO2-+2H2O.
点评 本题考查结构性质位置关系综合应用,比较基础,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:解答题
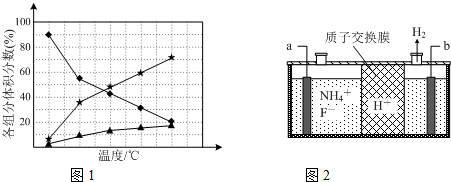
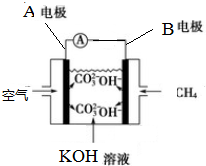 如图是一类甲烷燃烧电池示意图.
如图是一类甲烷燃烧电池示意图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②⑤ | C. | ②⑤⑥ | D. | ①④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
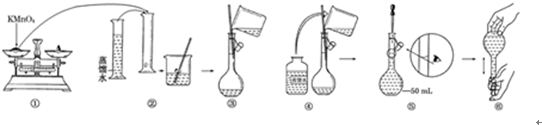
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到平衡时,SO2的浓度与SO3的浓度相等 | |
| B. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| C. | 为了提高SO2的转化率,应适当提高O2的浓度 | |
| D. | 在上述条件下,SO2不可能100%转化为SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑥ | B. | ①③⑤ | C. | ②④⑥ | D. | 以上全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z、N的简单离子的还原性:Z2->N- | |
| B. | Y2X和Y2X2都是碱性氧化物 | |
| C. | Z与X形成的化合物对应的水化物一定是强酸 | |
| D. | Z元素的非金属性比N元素的非金属性强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com