
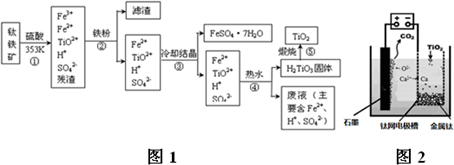
分析 第①步加硫酸溶解生成TiO2+和Fe2+、Fe3+等,第②步加铁粉还原Fe3+,过滤除去滤渣,第③步冷却结晶,过滤得到FeSO4•7H2O和含有TiO2+的溶液;第④步加热,热水使TiO2+水解生成H2TiO3,过滤得到H2TiO3;第⑤步H2TiO3受热分解生成化生成TiO2.
(1)铁粉将Fe3+转化为Fe2+;
(2)溶液中析出晶体是利用物质溶解度的不同得到;
(3)②③④都是从溶液中得到固体的分离过程,需要用过滤装置;
(4)依据溶液中存在平衡:TiO2++2H2O?H2TiO3+2H+,平衡影响因素和平衡移动原理分析判断;
(5)废液主要是亚铁离子、氢离子和二氧化锰反应发生氧化还原反应生成锰离子和铁离子;
(6)①依据装置图分析判断,阳极生成二氧化碳气体,是电解质中的氧离子失电子生成氧气,氧气和阳极石墨反应生成的二氧化碳;
②制备TiO2时,在电解槽发生如下反应:阴极:2Ca2++4e-═2Ca 阳极:2O2--4e-═O2↑,2Ca+TiO2$\frac{\underline{\;一定条件\;}}{\;}$Ti+2CaO,由此可见,CaO的量不变.
解答 解:(1)步骤②中,用铁粉将Fe3+转化为Fe2+的反应的离子方程式为:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe═3Fe2+;
(2)步骤③冷却结晶得到硫酸亚铁晶体,利用的是物质溶解度的不同,通过冷却热饱和溶液得到,故答案为:b;
(3)②③④步骤的操作过程中都得到沉淀或晶体,所以需要过滤得到固体和溶液,故答案为:过滤;
(4)④中使用热水的目的是促进TiO2+水解生成H2TiO3,分离出固体加热得到TiO2;溶液中存在平衡:TiO2++2H2O?H2TiO3+2H+,当加入热水稀释、升温后,
平衡正向移动,生成H2TiO3;
故答案为:溶液中存在平衡:TiO2++2H2O?H2TiO3+2H+,当加入热水稀释、升温后,平衡正向移动,生成H2TiO3.
(5)利用生产过程中的废液与软锰矿(主要成分为MnO2)反应生产硫酸锰(MnSO4,易溶于水),利用二氧化锰的氧化性氧化亚铁离子为三价铁离子,反应的离子方程式为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(6)①用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,阳极发生氧化反应,阴极析出钙金属发生还原反应,阳极图示产物可可知,阳极生成二氧化碳气体,是电解质中的氧离子失电子生成氧气,氧气和阳极石墨反应生成的二氧化碳,所以电极反应为:2O2--4e-=O2↑,或C+2O2--4e-=CO2↑;
故答案为:2O2--4e-=O2↑,或C+2O2--4e-=CO2↑;
②制备TiO2时,在电解槽发生如下反应:2CaO═2Ca+O2↑,2Ca+TiO2$\frac{\underline{\;一定条件\;}}{\;}$Ti+2CaO,由此可见,CaO的量不变;
或:制备TiO2时,在电解槽发生如下反应:阴极:2Ca2++4e-═2Ca,阳极:2O2--4e-═O2↑;2Ca+TiO$\frac{\underline{\;一定条件\;}}{\;}$Ti+2CaO,由此可见,CaO的量不变;
故答案为:制备TiO2时,在电解槽发生如下反应:2CaO═2Ca+O2↑,2Ca+TiO2$\frac{\underline{\;一定条件\;}}{\;}$Ti+2CaO,由此可见,CaO的量不变.
点评 本题考查了物质制备流程分析判断,为高考常见题型,综合考查实验基本操作,离子方程式的书写等,考查学生对所学知识的综合应用能力,注意物质分离的流程分析判断,物质性质的应用,题目难度中等


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:解答题
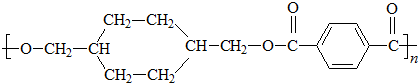
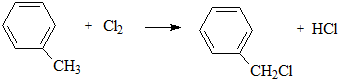
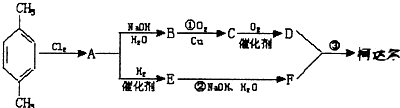
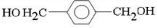 、D
、D 、E
、E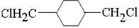 ;
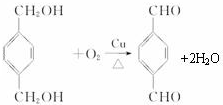
;
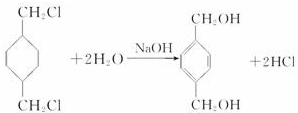 ;
; +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$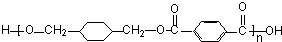 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
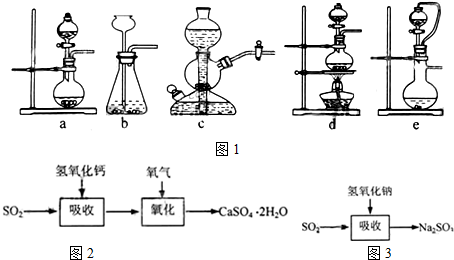
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.9 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾净水与液氯净水的原理相同 | |
| B. | 将草木灰和硫铵混合施用,肥效更高 | |
| C. | 冬季形成的大雾属于气溶胶 | |
| D. | 电解精炼铜时,同一时间内阴极溶解铜的质量比阳极析出铜的质量小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
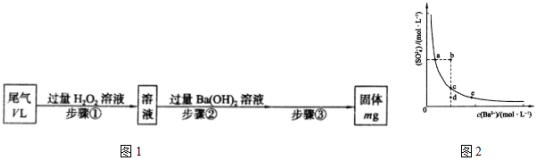
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 滤液A中的阳离子为Fe2+、Fe3+、H+ | B. | 样品CuO的质量一定为4.0g | ||
| C. | 样品中Fe元素的质量为56V/22400g | D. | 样品中Fe元素的质量为2.24 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
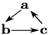 (“→”表示反应一步完成)关系转化的是( )
(“→”表示反应一步完成)关系转化的是( )| 选项 | a | b | c |
| A | NO | NO2 | HNO3 |
| B | SiO2 | Na2SiO3 | H2SiO3 |
| C | Al | NaAlO2 | Al(OH)3 |
| D | MgCl2 | Mg(OH)2 | MgO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
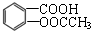 是一种常用的退热、镇痛药物,临床常用于预防心血管疾病.阿斯匹林对肠胃有一定的副作用,患有消化系统疾病的人不宜服用.则下列对此化合物说法不正确的是( )
是一种常用的退热、镇痛药物,临床常用于预防心血管疾病.阿斯匹林对肠胃有一定的副作用,患有消化系统疾病的人不宜服用.则下列对此化合物说法不正确的是( )| A. | 阿斯匹林能与NaHCO3反应,最多能与3mol H2发生加成反应 | |
| B. | 1 mol阿斯匹林与足量的NaOH溶液反应,消耗NaOH最大的物质的量为3 mol | |
| C. | 其苯环上的一氯取代物有两种 | |
| D. | 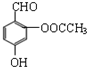 与阿斯匹林互为同分异构体,该有机物遇FeCl3溶液显紫色 与阿斯匹林互为同分异构体,该有机物遇FeCl3溶液显紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com