
下列说法正确的是
A.汽油、柴油、植物油都属烃类物质且均为纯净物
B.单质硅常用于制造芯片和光导纤维
C.等质量的气态乙醇和液态乙醇分别完全燃烧,前者放出的热量更多
D.漂白精和明矾都常用于自来水的处理,二者作用原理相同
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源:2013-2014湖南省衡南县高一下学期期末考试化学试卷(解析版) 题型:选择题
将0.2 mol下列烃完全燃烧后,生成的气体缓缓通过0.5 L 2mol/L的NaOH溶液中,生成正盐和酸式盐的物质的量之比为1:3,则该烷烃是( )
A.乙烷 B.丙烷 C.丁烷 D.戊烷
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省益阳市高一上学期期末考试化学(理)试卷(解析版) 题型:填空题
下表是元素周期表的一部分
周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① |
| |||||
2 | ② |
|
| ③ | ④ | ⑤ |
|
3 | ⑥ | ⑦ | ⑧ |
|
| ⑨ | ⑩ |
(1)在上述元素中,金属性最强的是 ,⑥~⑩中原子半径最小的是 (均填元素符号)
(2)表中元素⑩的氢化物的热稳定性比元素⑨的氢化物的热稳定性 (填“强”或“弱”)
(3)⑧号元素的最高价氧化物对应的水化物的化学式为 ,它与⑥号元素的最高价氧化物对应的水化物反应的离子方程式为 (3分)
(4)下列结构图中,大黑点(●)代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点未用于形成共价键的最外层电子,短线代表共价键。

根据各图表示的结构特点,写出各分子的化学式:
A: ,B: ,C: ,D 。(各1分)
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省怀化市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
(15分)【化学—选修5:有机化学基础】
已知有机物A~I之间的转化关系如下图所示:
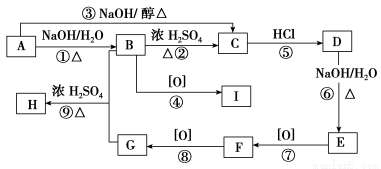
已知:
①A与D、B与E、I与F互为同分异构体
②将新制Cu(OH)2悬浊液分别加入到有机物I、F中,加热,I无明显现象,F反应并生成砖红色物质
③C的实验式与乙炔相同,且相对分子质量为104
④E的一种同分异构体与FeCl3能发生显色反应
根据以上信息,回答下列问题:
(1)H、 F中含有的含氧官能团名称分别为 、 。
(2)反应①~⑨中属于消去反应的是____________________________。
(3)I的结构简式为____________________________。
(4)写出H在酸性条件下水解的化学方程式 。
(5)写出F与银氨溶液反应的化学方程式 。
(6)符合以下条件的G的同分异构体有________种;其中苯环上只有2种一元取代物的结构简式为 。
①属于芳香族化合物
②能与NaOH溶液反应
③能发生银镜反应
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省怀化市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
已知氧化性:HClO>Cl2>Fe3+>SO42-;常温下,电离常数:K(H2CO3)>K(HClO)>K(HCO3-)>KAl(OH)3;则下列相关离子方程式正确的是
A.0.5mol/L的NaHSO3溶液与1.0mol/L的NaClO溶液等体积混合:HSO3-+ClO-=SO42-+Cl-+H+
B.小苏打溶液与偏铝酸钠溶液混合:HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
C.“84”消毒液(主要成分为NaClO)露置在空气中变质:2ClO-+CO2+H2O=CO32-+2HClO
D.在“84”消毒液中滴加FeSO4溶液:2Fe2++ClO-+H2O=2Fe3++Cl-+2OH-
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省怀化市高三第三次模拟考试理综化学试卷(解析版) 题型:填空题
已知;①Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K;
FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K;
②Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=b kJ·mol-1。
测得在不同温度下,K值如下:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
(1)反应①为__________(选填“吸热”或“放热”)反应。
(2)若500 ℃时进行反应①,CO2的起始浓度为2 mol·L-1,CO的平衡浓度为 。
(3)下列关于反应①的说法正确的是 。
A.达到平衡后保持其他条件不变,升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
B. 在500 ℃下反应,当c(CO2)=c(CO)时,反应达到平衡状态
C.恒温恒容下,当容器内气体密度不再变化时,反应达到平衡状态
D.加压、升温和使用催化剂均可增大反应物的转化率
(4)由已知反应,写出Fe2O3(s)被CO(g)还原成FeO(s)的热化学方程式 。
(5)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+开始沉淀;当溶液pH为4时,c(Fe3+)=__________mol·L-1(已知:Ksp[Fe(OH)3]=4.0×10-36)。
(6)新型锌空电池与锂电池相比,具有能量密度高、安全性好且成本低。该电池的总反应为2Zn+O2===2ZnO,电解质溶液为KOH溶液,则负极的电极反应式为_______。
若以该电池为电源,用惰性电极电解硫酸铜溶液,为保证阴极有6.4g铜析出,理论上至少需要标准状况下 L空气(空气中含氧气按20%计算)进入该电池。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省怀化市高三第三次模拟考试理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列叙述正确的是
A.14 gC2H4和C3H6的混合气体中含有的原子数为3NA
B.25 ℃时,1 L pH=13的氢氧化钡溶液中含有0.2NA个氢氧根离子
C.5.6克铁与一定量稀硝酸完全反应,电子转移数目一定为0.3NA
D.1.0L1mol/L的NaOH水溶液中含有的氧原子数目为2 NA
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省五市十校高一下学期期中教学质量检测化学试卷(解析版) 题型:填空题
将一螺旋状的铜丝放在酒精灯上灼烧,然后将热的铜丝插入盛有乙醇的试管中。整个反应过程中铜丝表面的颜色变化是 ,反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南师大附中第二学期期中考试高二化学试卷(解析版) 题型:选择题
已知卤代烃可以和钠发生反应,例如溴乙烷与钠发生反应为:
2CH3CH2Br+2Na―→CH3CH2CH2CH3+2NaBr;应用这一反应,下列所给化合物中可以与钠合成环丁烷的是
A.CH3Br B.CH3CH2CH2CH2Br
C.CH2BrCH2BrD.CH3CHBrCH2CH2Br
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com