
把0.05molNaOH固体分别加入下列100mL溶液中,溶液的导电能力变化不大的是()
A. 自来水 B. 0.5mol•L﹣1KOH溶液
C. 0.5mol•L﹣1醋酸 D. 0.5mol•L﹣1NH4Cl溶液
考点: 电解质与非电解质.
专题: 电离平衡与溶液的pH专题.
分析: 溶液混合后导电能力变化的大小,关键是看混合后溶液中自由移动的离子浓度的变化.
A.水是极弱的电解质,加入NaOH后为强电解质的溶液,导电性变化大;
B.0.5mol•L﹣1KOH溶液为强电解质溶液,当加入NaOH后,离子浓度增大很多,导电性变化大;
C.0.5mol•L﹣1醋酸为弱电解质溶液,当加入NaOH后,反应生成乙酸钠和水,离子浓度增大很多,成为强电解质溶液,导电性变化大;
D.氯化铵为强电解质溶液,加入NaOH后生成物NaCl仍是强电解质溶液,NH3•H2O为弱电解质,离子浓度变化不大,导电能力变化不大;
解答: 解:导电能力的大小与单位体积内离子浓度的多少成正比,溶液混合后导电能力变化的大小,关键是看混合后溶液中自由移动的离子浓度的变化.
A.因水是极弱的电解质,导电性极弱,加入氢氧化钠后,氢氧化钠是强电解质,溶液中主要的是钠离子和氢氧根离子,导电性增强,故A错误;
B.0.5mol•L﹣1KOH溶液,未加氢氧化钠固体,导电的有钾离子和氢氧根离子,加入氢氧化钠后主要是钠离子,氢氧根离子,离子浓度增大很多,所以导电性变化大,故B错误;
C.0.5mol•L﹣1醋酸原来是弱电解质,离子较少,加入强碱以后,变为强电解质,导电能力增强,所以导电性变化大,故C错误;
D.0.5mol•L﹣1氯化铵为强电解质,加入NaOH后,NH4Cl+NaOH=NaCl+NH3•H2O,未反应的氯离子,而参加反应的氨根离子正好与加入的钠离子的量相当,氨水为弱电解质,离子的浓度变化不大,故导电性变化不大,故D正确;
故选D.
点评: 本题考查溶液中离子浓度大小与溶液的导电性关系,溶液混合后导电能力变化的大小,关键是看混合后溶液中自由移动的离子浓度的变化,题目难度中等.


科目:高中化学 来源: 题型:
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此,下列说法正确的是( )

-A.-该硫酸的物质的量浓度为9.2mol•L﹣1
-B.-配制250mL4.6mol•L﹣1的稀硫酸需取该浓硫酸62.5mL
-C.-该硫酸浓度太大,不能用于干燥氨气
-D.-该硫酸与等质量的水混合后所得溶液的物质的量浓度等于9.2mol•L﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
在20g密度为d g/cm3的硝酸钙溶液里含1g Ca2+,则硝酸根离子的物质的量浓度是( )
|
| A. |
| B. |
|
|
| C. | 1.25d mol•L﹣1 | D. | 2.5d mol•L﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在给定的四种溶液中加入以下各种离子,各离子能在原溶液中共存的是()
A. 滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl﹣、SCN﹣
B. pH为1的溶液:Cu2+、Na+、Mg2+、NO3﹣
C. 水电离出来的c(H+)=10﹣13mol/L的溶液:K+、HCO3﹣、Br﹣、Ba2+
D. 所含溶质为Na2SO4的溶液:K+、CO32﹣、NO3﹣、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状态下,气态分子断开1mol化学键的焓变为键焓.已知H﹣H,H﹣O和O=O键的键焓△H分别为436kJ•mol﹣1、463kJ•mol﹣1和495kJ•mol﹣1.下列热化学方程式正确的是()
A. H2O(g)═H2(g)+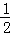 O2(g)△H=﹣485kJ•mol﹣1
O2(g)△H=﹣485kJ•mol﹣1
B. H2O(g)═H2(g)+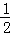 O2(g)△H=+485kJ•mol﹣1
O2(g)△H=+485kJ•mol﹣1
C. 2H2(g)+O2(g)═2H2O(g)△H=+485kJ•mol﹣1
D. 2H2(g)+O2(g)═2H2O(g)△H=﹣485kJ•mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中粒子的物质的量浓度关系正确的是()
A. 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32﹣)>c(HCO3﹣)>c(OH﹣)
B. 20mL 0.1mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO﹣)>c(Cl﹣)>c(CH3COOH)>c(H+)
C. 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl﹣)+c(H+)>c(NH4+)+c(OH﹣)
D. 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH﹣)>c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)⇌2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量).下列判断正确的是()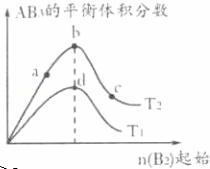
A. 若T2>T1,达到平衡时b、d点的反应速率为vd>vb
B. 若T2>T1,则正反应一定是放热反应
C. 达到平衡时A2的转化率大小为b>a>c
D. 在T2和n(A2)不变时达到平衡,AB3的物质的量大小为c>b>a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com