
在10L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,发生反应:
SO2(g)+ NO2(g) 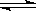 SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
试求:该温度下、该容器中,再继续加入1mol的SO2(g),则:
(1)化学平衡将向________方向移动,NO2的转化率将____________;
(2)经计算,当达到新的平衡状态时,容器中SO2(g)的浓度是_______mol/L;
(3)整个过程中,SO2的转化率由50%变为_______%,NO2的转化率由__________%变为_______%。
(4)计算结果给我们的启示是:增大一种反应物物的用量,其转化率将________________(填“增大” 、“不变”或“减小”)另一反应物的转化率将____________(填“增大” 、“不变”或“减小”)。现实生产中的意义是:可以通过增大________的用量,来提高成本高的反应物的利用率。
科目:高中化学 来源: 题型:
将0.2mol两种气态烃组成的混合气体完全燃烧后得到(标准状况下)6.72L二氧化碳和7.2g水, 下列说法正确的是( )
A.一定有乙烯 B.可能有乙烯 C.一定没有甲烷 D.可能有乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
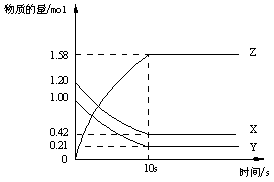
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
下列描述正确的是( )
A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
 D.反应的化学方程式为: X(g)+Y(g)
D.反应的化学方程式为: X(g)+Y(g)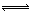 Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
对于平衡体系mA(气)+nB(气) PC(气)十qD(气) △H <0,有下列判断,其中正确的是
 A.若温度不变,将容器的体积缩小1倍,此时A的浓度变为原来的1 .8倍,则m+n<p+q
A.若温度不变,将容器的体积缩小1倍,此时A的浓度变为原来的1 .8倍,则m+n<p+q
B.若平衡时,A、B的转化率相等,说明反应开始时A,B的物质的量之比为m:n
C.若平衡体系共有气体amol,再向其中加人bmolB,当重新达到平衡时,气体的总物质的量等于(a+b),则m+n>p+q
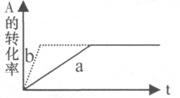
D.加催化剂或增大压强,可实现右图a→b的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
“嫦娥奔月”是一个充满浪漫主义的中国神话故事。2007年10月24日我国“嫦娥一号”探月卫星由长三甲火箭送入预定的轨道。长三甲火箭第三级推进剂采用低温液氧/液氢。已知在298K时,2g氢气与氧气完全反应生成液态水放热285.8kJ,则此反应的热化学方程式为
A.2H2(g)+O2(g) === 2H2O(l) △H=-285.8KJ·mol-1
B.2H2(g)+O2(g) === 2H2O(l) △H=+285.8KJ·mol-1
C.H2(g)+ O2(g) === H2O(l) △H=-285.8KJ·mol-1
O2(g) === H2O(l) △H=-285.8KJ·mol-1
D.H2(g)+  O2(g) === H2O(g) △H=-285.8KJ·mol-1
O2(g) === H2O(g) △H=-285.8KJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将0.1 mol·L-1NaOH溶液与0.06 mol·L-1 H2SO4溶液等体积混合,该混合溶液的pH等于
A.1.7 B.2.0 C.12.0 D.12.4
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗2-3次后,向其中注入0.1000 mol·L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2 mL。
 试回答下列问题:
试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
(2)该小组在步骤①中的错误是 ,
由此造成的测定结果 (偏高、偏低或无影响)。
(3)右图,是某次滴定时的滴定管中的液面,其读数为 mL。
(4)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |
请计算待测烧碱溶液的浓度为 mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知同一碳原子连有两个羟基不稳定: 。下列有关有机物
。下列有关有机物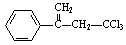 的说法不正确的是
的说法不正确的是
A.属于卤代烃,能使酸性高锰酸钾溶液和溴水褪色
B.该物质存在顺反异构
C.在碱性条件下充分水解,可生成羧酸盐
D.1mol 该物质在一定条件下可与4molH2发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com