
【题目】化学实验在学科中有着非常重要的作用,结合图示实验装置,下列相关分析的描述不正确的是( )
A.图1:盐桥中使用KCl溶液,电子的流向是Zn→G→Cu→CuSO4溶液→盐桥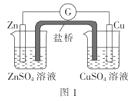
B.图2:可根据该实验验证铁的吸氧腐蚀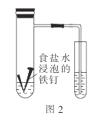
C.图3:在强酸和强碱的中和热实验中,强碱的浓度比强酸的略大
D.图4:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断反应2NO2(g)![]() N2O4(g)是一个放热反应
N2O4(g)是一个放热反应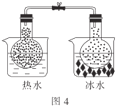
【答案】A
【解析】
A.图1表示的Zn-Cu原电池,Zn失去电子,作负极,电子经过外电,达到正极,电子流向为Zn→G→Cu,但是电子不能经过电解质溶液,也不能经过盐桥,错误,A符合题意;
B.若发生吸氧腐蚀,O2+4e-+2H2O=4OH-,装置中氧气的量减少,右侧导管中的液面会上升,可以证明发生了吸氧腐蚀,正确,B不符合题意;
C.在进行中和热的测定实验时,为了保证强酸完全反应掉,强碱的浓度会比强酸的略大,正确,C不符合题意;
D.根据图示,热水中的烧瓶的颜色更深,NO2的含量很多,可知,升高温度,平衡向着生成NO2的方向移动,则生成NO2的方向为吸热反应方向,可知2NO2(g)![]() N2O4(g)是一个放热反应,正确,D不符合题意。
N2O4(g)是一个放热反应,正确,D不符合题意。
答案选A。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】Li2CO3是生产锂电池的重要原料,电解铝废渣(主要含AlF3、LiF、NaF、CaO等物质)可用于制备Li2CO3。
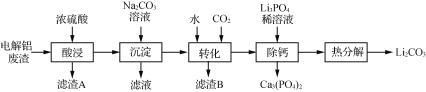
已知:①Li2CO3的溶解度:0 ℃ 1.54 g;20 ℃ 1.33 g;80 ℃ 0.85 g。
②20 ℃,Ksp[Ca3(PO4)2]=2×10-33,Ksp(CaHPO4)=1×10-7。
(1)在加热条件下酸浸,反应生成能腐蚀玻璃的气体,写出AlF3发生反应的化学方程式:______。

(2)滤渣B的主要成分是________。
(3)“转化”后所得LiHCO3溶液中含有的Ca2+需要加入Li3PO4除去。除钙步骤中其他条件不变,反应相同时间,温度对除钙率和Li2CO3产率的影响如右图所示。
①随着温度升高最终Li2CO3的产率逐渐减小的原因是___________。
②当温度高于50 ℃时,除钙率下降的原因可能是__________________。
(4)热分解后,获得Li2CO3需趁热过滤的原因是_______________________。
(5)将酸浸时产生的气体通入Al(OH)3和Na2SO4溶液的混合物中可产生难溶物冰晶石(Na3AlF6),该反应的离子方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨反应![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g) ![]() NH3(g) △H 的反应机理如图所示,图中“吸”表示各气态物质在催化剂表面吸附。下列说法错误的是
NH3(g) △H 的反应机理如图所示,图中“吸”表示各气态物质在催化剂表面吸附。下列说法错误的是
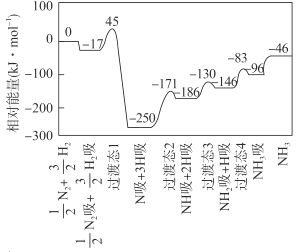
A.该反应的△H = -46 kJ·mol- 1
B.该反应机理中最大活化能为79 kJ·mol- 1
C.升高温度,该反应过渡态的能量会增大
D.该反应达到平衡后增大压强反应正向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
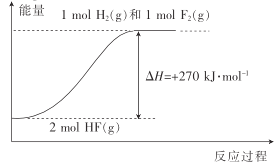
【题目】已知:H2(g)+F2(g)=2HF(g) △H1=-270kJmol-1。下列说法不正确的是( )
A.1molH2(g)与1molF2(g)的键能之和比2molHF(g)的键能高270kJ·mol-1
B.HF(g)分解为H2(g)与F2(g)的反应过程的能量变化可用如图来表示
C.若反应中有20gHF(g)生成,则放出135kJ热量
D.若H2(g)+Cl2(g)=2HCl(g) △H2=-QkJ·mol-1,则Q<270
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在相应的条件下能大量共存的是( )
A.由水电离产生的c(H+)=1×10-10molL-1的溶液中:NO3-、Fe2+、Na+、SO42-
B.![]() =10-10molL-1的溶液中:NH4+、I-、Cl-、K+
=10-10molL-1的溶液中:NH4+、I-、Cl-、K+
C.![]() =1×106的溶液中:K+、Na+、Cl-、HCO3-
=1×106的溶液中:K+、Na+、Cl-、HCO3-
D.惰性电极电解AgNO3后的溶液中:SO32-、K+、Na+、S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用所学知识,解决下列问题。
(1)AlCl3溶液呈___(填“酸”“中”或“碱”)性,原因是___(用离子方程式表示)。实验室配制AlCl3溶液时,常将AlCl3固体先溶于较浓的盐酸中,再用蒸熘水稀释到所需的浓度,目的是___。
(2)今有常温下五种溶液:CH3COONa溶液、NH4Cl溶液、NaOH溶液、氨水、NH4HSO4溶液。
①CH3COONa溶液pH___(填“>”“=”或“<” )7,若要使溶液的pH增大,可采取的措施是___。
②pH相等的NaOH溶液和CH3COONa溶液,分别稀释相同倍数后,NaOH溶液的pH___(填“>”“=”“<”)CH3COONa溶液。
③物质的量浓度均为0.1mol·L-1的三种溶液:A.NH4Cl溶液 B.NH4HSO4溶液 C.氨水,c(NH4+)由大到小的顺序为___(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ka(CH3COOH)=1.8×10-5,分别向20 mL 0.1 mol/L NaHCO3溶液和CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液,滴定曲线如图所示。下列叙述正确的是
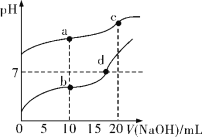
A.b点溶液中粒子浓度大小关系:c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH)>c(OH-)
B.c点溶液中存在:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-)
C.溶液中由水电离出c(H+)大小关系:b<d<a=c
D.d点溶液中: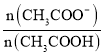 =180
=180
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有五种短周期元素,它们的结构、性质等信息如下表所示:
元素 | 结构、性质等信息 |
A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
C | 其气态氢化物极易溶于水,液态时常用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的杀菌消毒剂 |
E | 元素原子的L电子层上有2对成对电子 |
请根据表中信息回答下列问题。
(1)A元素原子的核外电子排布式为___。
(2)B元素在元素周期表中的位置为___;离子半径:B___(填“>”或“<”)A。
(3)C元素原子的轨道表示式为___,其原子核外有___个未成对电子,能量最高的电子排布在轨道上,该轨道呈___形。
(4)D元素原子的核外电子排布式为___,D-的结构示意图为___。
(5)C、E元素的第一电离能的大小关系是___(用元素符号表示)。
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是CD3___(用元素符号表示),CD3与水反应后的产物是___(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com