

 (4)含铬化合物有毒,对人畜危害很大.因此含铬废水必须进行处理才能排放.
(4)含铬化合物有毒,对人畜危害很大.因此含铬废水必须进行处理才能排放.


 SO3 + NO
SO3 + NO

 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.24 g NaH中阴离子所含电子总数为NA |
| B.标准状况下,22.4 L苯中含有C—H键数目为6NA |
C.在碳酸钠溶液中,若c(C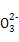 )="1" mol/L,则c(Na+)="2" mol/L )="1" mol/L,则c(Na+)="2" mol/L |
| D.通过MnO2催化使H2O2分解,产生32 g O2时转移电子数为2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 NH4++OH-,NaOH晶体使该可逆反应的平衡向左移动
NH4++OH-,NaOH晶体使该可逆反应的平衡向左移动

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 mol过氧化钡(BaO2)晶体中所含有的阴离子数目为2NA |
| B.标准状况下,22.4 L四氯化碳中所含有的共价键数目为4NA |
| C.将1 mol FeCl3转化为氢氧化铁胶体,得到的氢氧化铁胶体粒子数小于NA |
| D.常温常压下,33.6 L氯气与56 g铁充分反应,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.③④ | C.①③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.5 mol NO2与足量的H2O反应,转移的电子数为NA |
| B.常温常压下,0.5NA个CO2分子质量为22 g |
| C.28 g氮气所含的原子数目为NA |
| D.在标准状况下,0.5NA个氯气分子所占体积是11.2 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com