
【题目】将一小块金属钠长期露置于空气中发生一系列变化,最终产物是( )
A.NaOH
B.Na2O
C.Na2O2
D.Na2CO3
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】将一定质量的Na2CO3和NaHCO3混合物灼烧至恒重,将放出的气体通入足量的澄清石灰水中,充分反应后得到的沉淀的质量是l.0g,加热后剩余的固体物质与足量的稀盐酸反应,收集到1.12L气体(标准状况).则原固体混合物中NaHCO3的物质的量为_______,Na2CO3的质量为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工厂中用稀硫酸浸泡某矿石后的溶液中,除了含有大量硫酸外,还含有少量NH![]() 、Fe3+、AsO
、Fe3+、AsO![]() 、Cl-。为除去杂质离子,部分操作流程如下:
、Cl-。为除去杂质离子,部分操作流程如下:
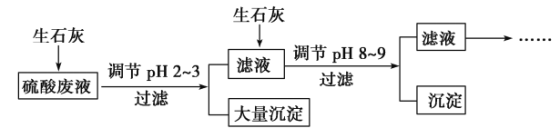
请回答问题:
(1)用稀硫酸浸泡某矿石后的溶液中,硫酸的浓度为4.9 g·L-1,则该溶液中的pH约为_____________________________。
(2)NH![]() 在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在。现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH
在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在。现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH![]() )恰好是NH4Cl溶液中c(NH
)恰好是NH4Cl溶液中c(NH![]() )的2倍,则c[(NH4)2SO4]__________c(NH4Cl)(填“<”“=”或“>”)。
)的2倍,则c[(NH4)2SO4]__________c(NH4Cl)(填“<”“=”或“>”)。
(3)随着向废液中投入生石灰(忽略溶液温度的变化),溶液中![]() __________(填“增大”“减小”或“不变”)。
__________(填“增大”“减小”或“不变”)。
(4)投入生石灰调节pH到2~3时,大量沉淀主要成分为CaSO4·2H2O[含有少量Fe(OH)3],提纯CaSO4·2H2O的主要操作步骤:向沉淀中加入过量________,充分反应后,过滤、洗涤、__________________________。
(5)25 ℃,H3AsO4电离常数为K1=5.6×10-3,K2=1.7×10-7,K3=4.0×10-12。当溶液中pH调节到8~9时,沉淀主要成分为Ca3(AsO4)2。
①pH调节到8左右Ca3(AsO4)2才开始沉淀的原因是_____________________。
②Na3AsO4第一步水解的平衡常数数值为___________________。
③已知:AsO![]() +2I-+2H+===AsO
+2I-+2H+===AsO![]() +I2+H2O,SO2+I2+2H2O===SO
+I2+H2O,SO2+I2+2H2O===SO![]() +2I-+4H+。上述两个反应中还原性最强的微粒是__________。
+2I-+4H+。上述两个反应中还原性最强的微粒是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学购买了一瓶“84消毒液”,包装说明如下:
净含量:1 000 mL 密度:1.19 g·cm-3
主要成分:25%NaClO
使用方法:稀释100倍(体积比)后使用
注意事项:密封保存,易吸收空气中的CO2变质
请根据以上信息和相关知识判断,下列分析不正确的是( )
A.该“84消毒液”的物质的量浓度约为4.0 mol·L-1
B.一瓶该“84消毒液”能吸收空气中44.8 L的CO2(标准状况)而变质
C.取100 mL该“84消毒液”稀释100倍后用以消毒,稀释后的溶液中c(Na+)约为0.04 mol·L-1
D.参阅该“84消毒液”的配方,欲用NaClO固体配制含25%NaClO的消毒液480 mL,需要称量的NaClO固体质量为143 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向MgSO4和Al2(SO4)3的混合溶液中, 逐滴加入NaOH溶液。下列图象中(横坐标表示NaOH溶液的体积, 纵坐标表示沉淀质量), 能正确表示上述反应的是 ( )

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.5.4 g Al分别与含溶质0.2 mol的NaOH溶液、盐酸反应,生成H2的分子数均为0.3NA
B.5.35 g NH4Cl固体中含有N—H键的个数为0.4NA
C.将含有1 mol FeCl3的浓溶液全部制成胶体,含Fe(OH)3胶粒的数目为NA
D.120 g熔融的NaHSO4中含阳离子总数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com