
【题目】如图所示装置中,金属镁、铝和电流表通过导线相连: 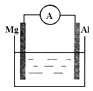
(1)若烧杯中溶液为稀硫酸,两极的电极反应式为: 负极;
正极 .
(2)若烧杯中溶液为氢氧化钠溶液,两极的电极反应式为: 负极;
正极 .
【答案】
(1)Mg﹣2e﹣=Mg2+;2H++2e﹣=H2↑
(2)Al+4OH﹣﹣3e﹣=AlO2﹣+2H2O;2H2O+2e﹣=H2↑+2OH﹣
【解析】解:(1)镁、铝和稀硫酸构成了原电池,金属镁做负极,电极反应:Mg﹣2e﹣=Mg2+ , 金属铝为正极,溶液中的2H+得到电子发生还原反应,电极反应为:2H++2e﹣=H2↑; 所以答案是:Mg﹣2e﹣=Mg2+;2H++2e﹣=H2↑.(2)镁、铝和NaOH溶液构成了原电池,铝易失电子作负极,电极反应式为Al+4OH﹣﹣3e﹣=AlO2﹣+2H2O,正极上水得电子发生还原反应,电极反应式为2H2O+2e﹣=H2↑+2OH﹣ ,
所以答案是:Al+4OH﹣﹣3e﹣=AlO2﹣+2H2O;2H2O+2e﹣=H2↑+2OH﹣ .


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在室温下,下列关于电解质的说法中正确的是
A. 中和等体积、等浓度的氨水和氢氧化钠溶液至pH=7,前者消耗的盐酸多
B. 向NH4Cl溶液中加入少量等浓度的稀盐酸,则![]() 的值减小
的值减小
C. 向NaHS溶液中加入适量 KOH 后:c(Na+)=c(H2S)+c(HS-)+c(S2-)
D. 将a mol·L-1的醋酸与0.01 mol·L-1的氢氧化钠溶液等体积混合(忽略体积、温度变化),所得溶液中c(Na+)=c(CH3COO-),则醋酸的电离常数Ka=![]() (用含a的代数式表示)
(用含a的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利科学家使用普通氧分子和带正电荷的氧离子制造出了由4个氧原子构成的氧分子O4,下列说法正确的是
A. O4和O2互为同位素
B. 同温同压下,等体积的O4气体和O2气体含有相同的分子数
C. 18O是氧元素的一种核素,它的中子数是8
D. O4转化O2为物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据图分析回答下列问题:
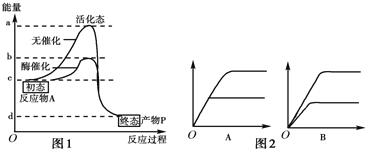
(1)酶所降低的活化能可用图1中 段来表示.如果将酶催化改为无机催化剂催化该反应,则b在纵轴上将 (上移/下移).
(2)图2纵轴为酶促反应速率,横轴为底物浓度,其中能正确表示酶量增加1倍时,底物浓度和反应速率关系的是 (填A或B).
(3)某实验小组为探究洗衣粉加酶后的洗涤效果,将一种无酶洗衣粉分成3等份,进行了3组实验.甲、乙组在洗衣粉中加入1种或2种酶,丙组不加酶,在不同温度下清洗同种化纤布上的2种污渍,其他实验条件均相同,下表为实验记录:

①甲组在洗衣粉中加入了 ;乙组在洗衣粉中加入了 .
②如果甲、乙和丙3组均在水温为80℃时洗涤同一种污渍,请比较这3组洗涤效果之间的差异并说明理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的图解表示构成细胞的元素、化合物及其作用,a、b、c、d、e代表不同的小分子物质,A、B、C、E代表不同的大分子物质,下列分析不正确的是( )
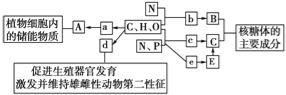
A. 在动物细胞内与A作用最相近的物质是糖原
B. 物质d的化学本质是固醇
C. e和c的区别是空间结构不同
D. 在人体细胞中物质e共有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
混合物 | 试剂 | 分离方法 | |
A | 苯(苯酚) | 溴水 | 过滤 |
B | 乙烷(乙烯) | 氢气 | 加热 |
C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
D | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 钠与水反应:Na+H2O===Na++OH-+H2↑
B. 稀硫酸与氢氧化钡溶液反应:H++OH-===H2O
C. 铁与氯化铁溶液反应:Fe+Fe3+===2Fe2+
D. 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O===2A1O![]() +3H2↑
+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 铵盐不稳定,受热分解都产生氨气
B. 向硅酸钠液中加适量稀盐酸,有透明的凝胶形成
C. 由于浓硫酸有强氧化性,因此不能用铁罐存浓硫酸
D. 浓硝酸不稳定,实验保存在无色试剂瓶中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com