
| A. | 晶格能大小:NaI>NaBr>NaCl>NaF | B. | 单质的熔点:Li<Na<K<Rb | ||
| C. | 共价键的键能:C-C>C-Si>Si-Si | D. | 沸点高低:HF<HCl<HBr<HI |
分析 A.离子晶体中晶格能与离子半径成反比、与电荷成正比;
B.金属晶体熔沸点与半径成反比;
C.键长越短键能越大;
D.氢化物中熔沸点与其相对分子质量成正比,但含有氢键的熔沸点较高.
解答 解:A.离子晶体中晶格能与离子半径成反比、与电荷成正比,这几种物质都是离子晶体,离子半径I->Br->Cl->F-,所以晶格能NaI<NaBr<NaCl<NaF,故A错误;
B.金属晶体熔沸点与半径成反比,碱金属元素原子半径随着原子序数增大而增大,所以其单质熔沸点随着原子序数增大而减小,故B错误;
C.键长越短键能越大,键长C-C<C-Si<Si-Si,则键能C-C>C-Si>Si-Si,故C正确;
D.氢化物中熔沸点与其相对分子质量成正比,但含有氢键的熔沸点较高,HF中含有氢键,熔沸点最高,所以熔沸点HCl<HBr<HI<HF,故D错误;
故选C.
点评 本题考查熔沸点高低判断,为高频考点,明确晶体类型及晶体熔沸点影响因素是解本题关键,注意氢键影响氢化物熔沸点,易错选项是D.


科目:高中化学 来源: 题型:解答题
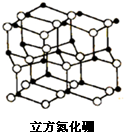 氮化硼是由氮原子和硼原子所构成的晶体,其组成为43.6%的硼和56.4%的氮(质量分数),有多种不同的变体,立方氮化硼是其中一种.立方氮化硼的硬度仅次于金刚石而远远高于其它材料,常用作磨料和刀具材料,其结构与金刚石类似(如图).
氮化硼是由氮原子和硼原子所构成的晶体,其组成为43.6%的硼和56.4%的氮(质量分数),有多种不同的变体,立方氮化硼是其中一种.立方氮化硼的硬度仅次于金刚石而远远高于其它材料,常用作磨料和刀具材料,其结构与金刚石类似(如图).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 1 | 2 | 3 | 4 |
| c(CH3COCH3)/mol•L-1 | 2.500 | 2.500 | 1.250 | 2.500 |
| c(HCl)/mol•L-1 | 0.500 | 1.000 | 1.000 | 1.000 |
| c(I2)/mol•L-1 | 0.010 | 0.010 | 0.010 | 0.020 |
| v(I2)/10-6 mol•L-1•s-1 | 1.500 | 3.000 | 1.498 | 3.000 |
| A. | I2的起始浓度越大,反应速率越大 | |
| B. | 该反应中HCl是催化剂,c(HCl)的改变不会影响反应速率 | |
| C. | 实验2与实验4两组实验的实验时间相等 | |
| D. | v(I2)/[c(CH3COCH3)•c(HCl)]为常数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BeF2分子中,中心原子Be的价层电子对数等于2,其空间排布为直线,成键电子对数也等于2 | |
| B. | BeF2分子的立体结构为直线形 | |
| C. | SF2分子中,中心原子S的价层电子对数等于4,其空间排布为四面体,成键电子对数等于2,没有孤对电子 | |
| D. | 在气相中,BeF2是直线形而SF2是V形 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
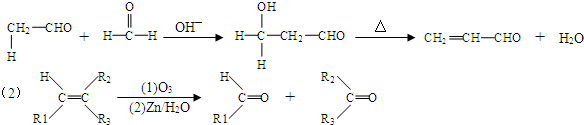
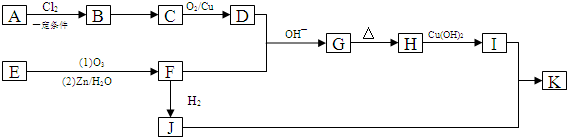
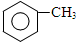 ,B→C的反应类型为:取代反应
,B→C的反应类型为:取代反应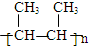
 +O2$→_{△}^{Cu}$ 2
+O2$→_{△}^{Cu}$ 2 +H2O;I+J→K:
+H2O;I+J→K: +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$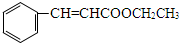 +H2O
+H2O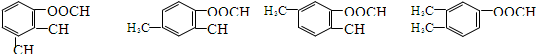 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采用原煤脱硫技术,可减少燃煤产生的SO2,从而有效降低酸雨的产生和危害 | |
| B. | FeCl2、CuS、SO3、NO2都不能由单质间直接化合得到 | |
| C. | SO2既可以由硫的化合物氧化得到,又可以由硫的化合物还原得到 | |
| D. | 硫为不溶于水,易溶于酒精和CS2的黄色粉末 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com