
| A、NH3 |
| B、CCl4 |
| C、SO32- |
| D、CH2O |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、第三周期主族元素的最高正价均等于其族序数 |
| B、短周期元素的简单离子,最外层电子均达到8电子稳定结构 |
| C、第ⅠA族元素也称碱金属元素,其原子最外层电子数均为1 |
| D、同一主族元素的原子,最外层电子数相同,化学性质完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下,原子数均为NA的氢气和氦气具有相同的体积 |
| B、常温常压下,17g甲基(-CH3)所含电子数为10NA |
| C、在密闭容器中,0.1mol O2和0.2mol SO2在催化剂作用下充分反应生成SO3的分子数为0.2NA |
| D、标况下,22.4L丙烷中共价键数目为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、红磷和白磷互称同位素 |
| B、相同量的白磷比红磷的总能量低 |
| C、该反应是吸热反应 |
| D、红磷比白磷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蛋白质在紫外线的照射下会失去生理活性 |
| B、蛋白质溶液不能产生丁达尔效应 |
| C、蛋白质溶液中加入CuSO4可产生盐析现象 |
| D、蚕丝、羊毛、棉花的主要成分都是蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH4+Cl2
| |||
B、CH3COOCH2CH3+H2O
| |||
C、 +HONO2 +HONO2
 +H2O +H2O | |||
D、2CH3CHO+O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
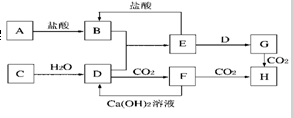
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com