
【题目】化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究。查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
I.摩擦剂中氢氧化铝的定性检验,取适量牙膏样品,加水充足搅拌、过滤。
(1)往滤渣中加入过量![]() 溶液,过滤。氢氧化铝与
溶液,过滤。氢氧化铝与![]() 溶液反应的离子方程式是___________
溶液反应的离子方程式是___________
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸,观察的现象是__________
Ⅱ.牙膏样品中碳酸钙的定量测定。利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的![]() 沉淀质量,以确定碳酸钙的质量分数。
沉淀质量,以确定碳酸钙的质量分数。
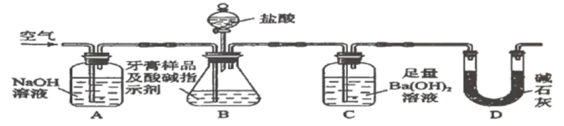
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:_____。
(4)C中反应生成沉淀的离子方程式是_______________。
(5)下列各项措施中,不能提高测定准确度的是________(填标号)。
a.在加入盐酸之前,应排净装置内的![]() 气体
气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取![]() 样品三份,进行三次测定,测得
样品三份,进行三次测定,测得![]() 平均质量为
平均质量为![]() 。则样品中碳酸钙的质量分数为_____________________。
。则样品中碳酸钙的质量分数为_____________________。
(7)有人认为不必测定C中生成的![]() 质量,只要测定装置C在吸收
质量,只要测定装置C在吸收![]() 前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是____________________。
前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是____________________。
【答案】![]() 通入CO2气体先没有现象后有白色沉淀生成,加入盐酸后先有气体产生,后有沉淀溶解; 在实验开始前先通空气,可排出装置内原空气中的CO2,实验结束后把B生成的CO2全部排入C中,使之完全被Ba(OH)2溶液吸收,减小误差
通入CO2气体先没有现象后有白色沉淀生成,加入盐酸后先有气体产生,后有沉淀溶解; 在实验开始前先通空气,可排出装置内原空气中的CO2,实验结束后把B生成的CO2全部排入C中,使之完全被Ba(OH)2溶液吸收,减小误差 ![]() cd 20.00% B中的水蒸气、氯化氢气体等进入装置C中,导致测定二氧化碳的质量偏大,测定的碳酸钙的质量偏大,碳酸钙的质量分数偏高
cd 20.00% B中的水蒸气、氯化氢气体等进入装置C中,导致测定二氧化碳的质量偏大,测定的碳酸钙的质量偏大,碳酸钙的质量分数偏高
【解析】
I.摩擦剂中氢氧化铝的定性检验主要围绕反应物的用量、固体或溶液中所含物质的性质回答;
Ⅱ.牙膏样品中碳酸钙的定量测定,实验原理是样品中的碳酸钙在过量HCl作用下转变成二氧化碳,二氧化碳再被过量氢氧化钡充分吸收得到碳酸钡沉淀,测定纯净而干燥的碳酸钡质量就可以计算出样品中碳酸钙的定量,据此回答;
Ⅰ.(1)氢氧化铝与NaOH溶液反应生成偏铝酸钠与水,反应离子方程式为:![]() ;
;
答案为:![]() ;
;
(2)滤液中含氢氧化钠和偏铝酸钠,先通入过量二氧化碳,氢氧化钠先与CO2发生反应,无明显现象,后![]() 出现沉淀,再加入过量稀盐酸, 溶液中的碳酸氢根离子先与氢离子反应
出现沉淀,再加入过量稀盐酸, 溶液中的碳酸氢根离子先与氢离子反应![]() ,放出气体,后发生
,放出气体,后发生![]() 反应,沉淀溶解;
反应,沉淀溶解;
答案为:先没有现象,而后有白色沉淀生成,加HCl先产生气泡,后沉淀全部溶解;
(3)未反应前装置内有空气,其中的二氧化碳会导致测定的碳酸钡的质量偏大,反应后装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小;
答案为:在实验开始前先通空气,可排出装置内原空气中的CO2,实验结束后把B生成的CO2全部排入C中,使之完全被Ba(OH)2溶液吸收,减小误差;
(4):二氧化碳与氢氧化钡反应生成碳酸钡与水,离子方程式为:![]() ;
;
答案为:![]() ;
;
(5) a. 在加入盐酸之前,应排净装置内的CO2气体,防止影响碳酸钡质量的测定,可以提高测定准确度,故a错误;
b. 滴加盐酸过快CO2,CO2来不及被吸收,就排出装置C,滴加盐酸不宜过快,使二氧化碳吸收完全,可以提高测定准确度,故b错误;
c. 在AB之间增添盛有浓硫酸的洗气装置,吸收水分,不影响CO2,不能提高提高测定准确度,故c正确;
d. 在BC之间增添盛有饱和碳酸氢钠溶液的洗气装置,CO2中混有的HCl与碳酸氢钠反应生成二氧化碳,影响了CO2的总量,不能提高测定准确度,故d正确;
答案为:cd;
(6) BaCO3质量为3.94g,则n(BaCO3)=![]() =0.02mol,则n(CaCO3)=0.02mol,质量为0.02mol×100g/mol=2.00g,所以样品中碳酸钙的质量分数为:
=0.02mol,则n(CaCO3)=0.02mol,质量为0.02mol×100g/mol=2.00g,所以样品中碳酸钙的质量分数为:![]() ;
;
答案为:20.00%;
(7) 碳酸钙的质量分数偏高,是因为杂质气体进入装置C,使测得的二氧化碳的质量偏大,杂质气体来自B中的水蒸气、氯化氢气体;
答案为:B中的水蒸气、氯化氢气体等进入装置C中,导致测定二氧化碳的质量偏大,测定的碳酸钙的质量偏大,碳酸钙的质量分数偏高。


科目:高中化学 来源: 题型:
【题目】接触法制硫酸的三个阶段:煅烧、氧化、吸收。煅烧黄铁矿的化学方程式为:
4FeS2 + 11O2 → 2Fe2O3 + 8SO2。
完成下列填空:
(1)煅烧黄铁矿在________(填设备名称)中进行,此反应中被氧化的元素是___________。
(2)SO2的催化氧化:2SO2(g)+O2(g)![]() 2SO3(g),该反应的平衡常数表达式为K= ______;反应达到平衡,及时分离出SO3,则平衡向_________方向移动(选填“正反应”“逆反应”)。其他条件不变,降低温度平衡向正反应方向移动,则正反应为__________反应(选填“吸热”“放热”)。
2SO3(g),该反应的平衡常数表达式为K= ______;反应达到平衡,及时分离出SO3,则平衡向_________方向移动(选填“正反应”“逆反应”)。其他条件不变,降低温度平衡向正反应方向移动,则正反应为__________反应(选填“吸热”“放热”)。
(3)下图为二氧化硫与氧气反应的速率(ν)与时间(t)的关系,判断在t1时刻曲线发生变化的原因是______(选填编号)。

a. 增大O2的浓度
b. 扩大容器体积
c. 加入催化剂
d. 升高温度
改变条件后,平衡混合物中SO3的百分含量_______(选填“增大”“减小”“不变”)。
(4)SO3的吸收:SO3 + H2O → H2SO4 。假定制备硫酸的整个过程中S元素共损失10%,则含1000 kg FeS2的黄铁矿可以制得98%的浓硫酸_____________kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两同学为制得纯净的Fe(OH)2,使用如图所示的装置,A管中是Fe和H2SO4,B管中是NaOH溶液:

(1)同学甲:先夹紧止水夹a,使A管开始反应,在B管中观察到的现象是___________;
(2)同学乙:打开a,使A管中反应一段时间后再夹紧止水夹a,实验中在B管中观察到的现象是___________,B中发生反应的离子方程式为____________________________________
(3)在制备纯净的Fe(OH)2实验中,一定要注意避免Fe(OH)2被氧化,一旦实验失败就会看到白色絮状沉淀逐渐变为灰绿色,最后变成红褐色,请写出这个过程的化学方程式,并用单线桥法标出电子转移的方向和数目:_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在平板电视显示屏生产过程中产生的废玻璃粉末中含有二氧化铈(CeO2)。
(1)在空气中煅烧Ce(OH)CO3可制备CeO2,该反应的化学方程式______________;
(2)已知在一定条件下,电解熔融状态的CeO2可制备![]() ,写出阳极的电极反应式:_______。
,写出阳极的电极反应式:_______。
(3)某课题组以上述废玻璃粉末(含有SiO2,Fe2O3,CeO2以及其它少量不溶于稀酸的物质)为原料,设计如图流程对资源进行回收,得到Ce(OH)4和硫酸铁铵。

①过滤得到滤渣B时,需要将其表面杂质洗涤干净,沉淀洗涤的的操作是_______。
②反应①的离子方程式为____________。
③操作I的名称是_____________。
④已知:M[Ce(OH)4]=208g/mol,氧化还原滴定法测定制得的Ce(OH)4产品纯度的流程为:称取0.600gCe(OH)4样品→加硫酸溶解→用0.1000mol/LFeSO4标准液滴定,消耗25.00mL标准液。该产品中Ce(OH)4的质量分数为____________(小数点后保留两位),若滴定所用FeSO4溶液己在空气中露置了一段时间,则测得该Ce(OH)4产品的纯度___________(“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铂钴合金是以铂为基含钴二元合金,在高温下,铂与钻可无限互溶,其固体为面心立方晶格。铂钻合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。氟及其化合物CuF用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________________方法区分晶体、准晶体和非晶体。
(2)基态F原子的价层电子排布图(轨道表达式)为________________。
(3) [H2F]+[SbF6]ˉ (氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为______________,与[H2F]+具有相同空间构型且中心原子与F原子同周期的分子是_____________。
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。![]() 中心原子的杂化类型是____________;氟化铵中存在_______________(填字母)。
中心原子的杂化类型是____________;氟化铵中存在_______________(填字母)。
A.离子键 B.σ键 C.π键 D.氢键
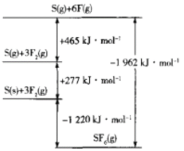
(5)SF4被广泛用作高压电气设备的绝缘介质。SF4是一种共价化合物,可通过类似于Bom-Haber循环能量构建能量图计算相关键能。则F-F键的键能为_____kJ/mol,S-F键的键能为______ kJ/mol。
(6)CuCl的熔点为326℃,能升华,熔化呈液态时不导电;CuF的熔点为1008℃,熔化呈液态时能导电。
①CuF中Cu+的基态价电子排布式________铜元素位于元素周期________区,金属Cu的堆积模型为__________________。
②CuF的熔点比CuCl的高,原因是______________
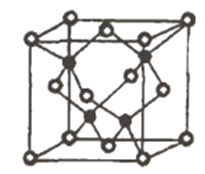
③已知NA为阿伏加德罗常数的值,CuF的密度为7.1g/cm3,晶胞结构如图所示,则CuF的晶胞参数a=_______nm(列出计算式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示;下列描述错误的是:

A. 淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
B. 以NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品
C. 步骤Ⅱ中鼓入热空气吹出溴,是因为溴蒸气的密度比空气的密度小
D. 用SO2水溶液吸收Br2的离子反应方程式为:Br2+SO2+2H2O═4H++SO42﹣+2Br﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的炭即可产生水煤气。反应为:
C(s)+H2O(g)![]() CO(g)+H2(g) ΔH= +131.3kJ/mol,ΔS= +133.7J/(K·mol)。
CO(g)+H2(g) ΔH= +131.3kJ/mol,ΔS= +133.7J/(K·mol)。
①该反应能否自发进行与________________有关。
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是________(填字母,下同)。
a.容器中的压强不变
b.1mol H-H键断裂的同时断裂2mol H-O键
c.v正(CO)=v逆(H2O)
d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)![]() CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验1中以v(CO2)表示的反应速率为__________。
②该反应的逆反应为________(填“吸”或“放”)热反应。
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3min,则a、b应满足的关系是____________________(用含a、b的数学式表示)。
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ/mol)的变化。在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使 c(CH3OH)增大的是___。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ/mol)的变化。在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使 c(CH3OH)增大的是___。
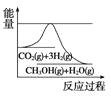
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来 d.再充入1mol CO2和3mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质、非电解质的说法正确的是:
A.氯气溶于水得氯水,该溶液能导电,因此氯气是电解质
B.CaCO3![]() 饱和溶液导电能力很弱,故CaCO3是弱电解质
饱和溶液导电能力很弱,故CaCO3是弱电解质
C.HF的水溶液中既有H+、F+,又有大量的HF分子,因此HF是弱电解质
D.导电能力弱的溶液肯定是弱电解质的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。结合氯气的物理性质,判断下列叙述中不正确是________________(填序号)。
MnCl2+Cl2↑+2H2O。结合氯气的物理性质,判断下列叙述中不正确是________________(填序号)。
①加热盛有二氧化锰、浓盐酸的烧瓶,瓶内充满黄绿色气体。
②氯气的密度比空气大,常用向上排空气法收集氯气。
③闻氯气气味时,用手轻轻在集气瓶口扇动,使极少量氯气飘进鼻孔。
④在充满氯气的集气瓶内加水,盖严后振荡,瓶内气体颜色变浅,液体变为黄绿色。
⑤氯气易液化,在低温和加压的条件下可以转变为液态(液氯)和固态。
⑥氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com