
【题目】某学生设计了四种实验方案并得出了自己的结论,其中实验方案设计及结论均正确的是( )
A. 淀粉溶液![]() 水解液溶液
水解液溶液![]() 变蓝。结论:淀粉完全没有水解
变蓝。结论:淀粉完全没有水解
B. 淀粉溶液![]() 水解液
水解液![]() 无砖红色沉淀。结论:淀粉完全水解
无砖红色沉淀。结论:淀粉完全水解
C. 淀粉溶液![]() 水解液
水解液![]() 中和液
中和液![]() 有砖红色沉淀。结论:淀粉已水解
有砖红色沉淀。结论:淀粉已水解
D. 淀粉溶液![]() 水解液
水解液![]() 无现象。结论:淀粉没有水解
无现象。结论:淀粉没有水解
科目:高中化学 来源: 题型:
【题目】(1)羟基的电子式________;
(2)﹣C3H7结构简式:________、________;
(3)CH3C(CH3)2CH2C(CH3)3系统命名为________该烃一氯取代物有________种。
(4)支链只有一个乙基且相对分子质量最小的烷烃的结构简式________。
(5)键线式 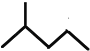 表示的分子式________。
表示的分子式________。
(6)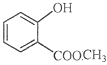 中含有的官能团的名称为________。
中含有的官能团的名称为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用如图装置进行中和热的测定。回答下列问题:
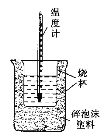
(1)该图中有两处未画出,它们是____________、____________。
(2)在操作正确的前提下提高中和热测定的准确性的关键是____________。
(3)如果用0.50 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将____________(填“偏大”、“偏小”或“不变”);原因是____________。
(4)乙醇是未来内燃机的首选环保型液体燃料。2.0g乙醇完全燃烧生成液态水放出59.43 kJ的热量,表示乙醇燃烧热的热化学方程式为____________________________。
(5)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2,其△H=__________kJ·mol-1。
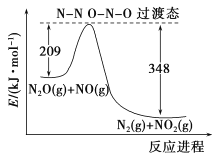
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化铵(NH4H)与氯化铵的结构相似,又知它与水反应有气体生成。下列关于氢化铵叙述正确的是( )
A.氢元素的化合价都是![]() 价B.电子式是
价B.电子式是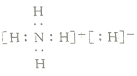
C.与水反应时,是氧化剂D.固体投入少量的水中,只产生一种气体NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )

A. 反应①为取代反应,反应需在光照条件下进行
B. 反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C. 反应③为取代反应,有机产物是一种烃
D. 反应④中1 mol苯最多与3 mol H2发生加成反应,是因为一个苯分子含有三个碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列有机物的官能团名称:
 _________________________
_________________________
(2)书写以下化学方程式
①乙烯与溴水的加成反应__________________________________________________
②氯乙烯的加聚反应______________________________________________________
③![]() 在碱性条件下的水解反应_________________________________
在碱性条件下的水解反应_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。常用的自来水消毒剂有二氧化氯(ClO2)和高铁酸钾(K2FeO4)等。
(1)某研究小组用下图装置制备少量ClO2(夹持装置已略去)。

资料:ClO2常温下为易溶于水而不与水反应的气体,水溶液呈深黄绿色,11℃时液化成红棕色液体。以NaClO3和HCl的乙醇溶液为原料制备ClO2的反应为2NaClO3 + 4HCl= 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O。
①冰水浴的作用是____________。
② NaOH溶液中发生的主要反应的离子方程式为________________。
(2)将ClO2水溶液滴加到KI溶液中,溶液变棕黄;再向其中加入适量CCl4,振荡、静置,观察到____,证明ClO2具有氧化性。
(3)ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO2-),需将其转化为Cl-除去。下列试剂中,可将ClO2-转化为Cl-的是_____________________(填字母序号)。
a. FeSO4 b. O3 c. KMnO4 d. SO2
(4)K2FeO4是一种新型、绿色的多功能净水剂,集氧化、吸附、絮凝、沉淀、灭菌、消毒、脱色、除臭等性能为一体。实验室制备K2FeO4的方法如下:在冰水浴中,向KClO和KOH的混合溶液中少量多次加入硝酸铁,并不断搅拌。
①上述制备K2FeO4反应的离子方程式为______________________。
②净水过程中,K2FeO4起到吸附、絮凝作用的原理是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲用固体NaOH配制100 mL 1 mol·L-1的NaOH溶液。
(1)用托盘天平称取NaOH固体的质量为____g
(2)下列情况使所配得溶液的浓度如何变化?(填“偏大”“ 偏小”或“不变”)
A.未洗涤溶解氢氧化钠的烧杯。____
B.容量瓶使用前用蒸馏水洗过,内壁附有水珠而未干燥处理。____
C.定容时加水超过了刻度线,将多出的液体吸出。____
D.定容时俯视容量瓶读数。____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个恒容容器中充入N2(g)和H2(g),一定条件下发生反应N2(g)+3H2(g)![]() 2NH3(g),若温度保持不变,下列说法正确的是( )
2NH3(g),若温度保持不变,下列说法正确的是( )
A.容器中的压强始终保持不变
B.反应达到限度后N2(g)和H2(g)的物质的量之比一定为1:3
C.正、逆反应速率相等时各物质质量不再变化
D.当充入足够N2(g)后,H2(g)会全部转化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com