
 £Ø1£©ŅŃÖŖH-H ¼üÄÜĪŖ436kJ•mol-1£¬H-N¼ü¼üÄÜĪŖ391kJ•mol-1£¬øł¾Ż»Æѧ·½³ĢŹ½£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.4kJ•mol-1£®ŌņN”ŌN¼üµÄ¼üÄÜŹĒ945.6 kJ/mol
£Ø1£©ŅŃÖŖH-H ¼üÄÜĪŖ436kJ•mol-1£¬H-N¼ü¼üÄÜĪŖ391kJ•mol-1£¬øł¾Ż»Æѧ·½³ĢŹ½£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.4kJ•mol-1£®ŌņN”ŌN¼üµÄ¼üÄÜŹĒ945.6 kJ/mol·ÖĪö £Ø1£©·“Ó¦ČČ=·“Ó¦ĪļµÄ×ܼüÄÜ-Éś³ÉĪļµÄ×ܼüÄÜ£¬ŅŌ“Ė½ā“š£»
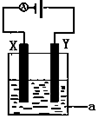
£Ø2£©ÄÜÉč¼Ę³ÉŌµē³ŲµÄ·“Ó¦Ķس£ŹĒ·ÅČČ·“Ó¦£¬ĒŅ±ŲŠėŹĒÄÜ×Ō·¢½ųŠŠµÄŃõ»Æ»¹Ō·“Ó¦£»
£Ø3£©Ōµē³ŲÖŠ£¬Õż¼«ÉĻŃõ»Æ¼ĮµĆµē×Ó·¢Éś»¹Ō·“Ó¦£»
£Ø4£©¢ŁČōµē½āĮņĖįĶČÜŅŗŹ±£¬Ńō¼«ÉĻĒāŃõøłĄė×ӷŵē£¬Ņõ¼«ÉĻĶĄė×ӷŵē£¬¾Ż“ĖŠ“³öµē³Ų·“Ó¦Ź½£¬øł¾ŻĶŗĶ×ŖŅʵē×ÓÕż¼«µÄ¹ŲĻµŹ½¼ĘĖć£»
¢Śøł¾Ż×ŖŅʵē×ÓŹŲŗć¼ĘĖćŅõ¼«ÉĻĪö³öµÄĪļÖŹ£¬ŌŁøł¾ŻŃõĘų¼ĘĖćÉś³ÉµÄC£ØH+£©£¬“Ó¶ųµĆ³öĘäpH£»
¢Ū¹¤Ņµ¾«Į¶ĶŹ±£¬Ńō¼«ŹĒ“ÖĶ£¬µē½āŅŗĪŖŗ¬ĶĄė×ÓµÄČÜŅŗ£®
½ā“š ½ā£ŗ£Ø1£©ŅŃÖŖ£ŗH-H¼üÄÜĪŖ436kJ/mol£¬H-N¼üÄÜĪŖ391kJ/mol£¬ĮīN”ŌNµÄ¼üÄÜĪŖx£¬
¶ŌÓŚ·“Ó¦N2£Øg£©+3H2£Øg£©=2NH3£Øg£©”÷H=-92.4kJ/mol£¬
·“Ó¦ČČ=·“Ó¦ĪļµÄ×ܼüÄÜ-Éś³ÉĪļµÄ×ܼüÄÜ£¬¹Źx+3”Į436kJ/mol-2”Į3”Į391kJ/mol=-92.4kJ/mol£¬
½āµĆ£ŗx=945.6 kJ/mol£¬¹Ź“š°øĪŖ£ŗ945.6 kJ/mol£»
£Ø2£©ÄÜÉč¼Ę³ÉŌµē³ŲµÄ·“Ó¦Ķس£ŹĒ·ÅČČ·“Ó¦£¬ĒŅ±ŲŠėŹĒÄÜ×Ō·¢½ųŠŠµÄŃõ»Æ»¹Ō·“Ó¦£¬
A£®øĆ·“Ó¦ŹĒĪüČČ·“Ó¦£¬ĖłŅŌ²»ÄÜÉč¼Ę³ÉŌµē³Ų£¬¹Ź²»Ń”£»
B£®øĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦ĒŅÄÜ×Ō·¢µÄ½ųŠŠŃõ»Æ»¹Ō·“Ó¦£¬ĖłŅŌÄÜÉč¼Ę³ÉŌµē³Ų£¬¹ŹŃ”£»
C£®øĆ·“Ó¦²»ŹĒŃõ»Æ»¹Ō·“Ó¦£¬ĖłŅŌ²»ÄÜÉč¼Ę³ÉŌµē³Ų£¬¹Ź²»Ń”£»
¹ŹŃ”£ŗB£»
£Ø3£©ŅŌKOHČÜŅŗĪŖµē½āÖŹČÜŅŗµÄĒāŃõČ¼ĮĻµē³ŲÖŠ£¬Õż¼«ÉĻŃõĘųµĆµē×ÓŗĶĖ®·“Ӧɜ³ÉĒāŃõøłĄė×Ó£¬µē¼«·“Ó¦Ź½ĪŖ£ŗO2+2H2O+4e-=4OH-£¬¹Ź“š°øĪŖ£ŗO2+2H2O+4e-=4OH-£»
£Ø4£©¢Łµē½āĮņĖįĶČÜŅŗŹ±£¬Ńō¼«ÉĻÉś³ÉŃõĘų£¬Ņõ¼«ÉĻÉś³ÉĶ£¬Ķ¬Ź±ČÜŅŗÖŠÉś³ÉĮņĖį£¬ĖłŅŌµē³Ų·“Ó¦Ź½ĪŖ£ŗ2CuSO4+2H2O$\frac{\underline{\;µē½ā\;}}{\;}$2Cu+O2”ü+2H2SO4£¬¹Ź“š°øĪŖ£ŗ2CuSO4+2H2O$\frac{\underline{\;µē½ā\;}}{\;}$2Cu+O2”ü+2H2SO4£»
¢Śµē½āŗ¬ÓŠ0.04molCuSO4ŗĶ0.04molNaClµÄ»ģŗĻČÜŅŗ400ml£¬Ńō¼«ÉĻĻČÉś³ÉĀČĘųŗóÉś³ÉŃõĘų£¬Ņõ¼«ÉĻĻČÉś³ÉĶ£¬ŗóÉś³ÉĒāĘų£¬Ńō¼«ÉĻĀČĘųĶźČ«Īö³öŹ±£¬ĀČĘųµÄĢå»ż=$\frac{0.04mol}{2}$=448mL£¼672mL£¬ĖłŅŌŃō¼«ÉĻ»¹ÓŠ224mLŃõĘų£¬Ńō¼«ÉĻ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæ=0.04mol”Į1+$\frac{0.224L}{22.4L/mol}$=0.08mol£¬Ņõ¼«ÉĻĶĶźČ«Īö³öŹ±£¬ŠčŅŖµē×ÓµÄĪļÖŹµÄĮæ=0.04mol”Į2=0.08mol£¬ĖłŅŌŅõ¼«ÉĻ²»Īö³öĒāĘų£¬Éś³É224mLŃõĘųŹ±£¬Ńō¼«ø½½üĶ¬Ź±Éś³ÉC£ØH+£©=$\frac{\frac{0.224}{22.4}mol”Į4}{0.4L}$=0.1mol/L£¬ĖłŅŌČÜŅŗµÄpH=1£¬¹Ź“š°øĪŖ£ŗ1£»
¢Ū¹¤Ņµ¾«Į¶ĶŹ±£¬Ńō¼«ŹĒ“ÖĶ£¬µē½āŅŗĪŖŗ¬ĶĄė×ÓµÄČÜŅŗCuSO4»ņCuCl2£¬¹Ź“š°øĪŖ£ŗCuSO4»ņCuCl2£»Y£®
µćĘĄ ±¾Ģā漲鹹³ÉŌµē³ŲµÄĢõ¼ž”¢µē½ā³ŲµÄÓŠ¹Ų¼ĘĖćµČÖŖŹ¶µć£¬ÄѵćŹĒ£Ø4£©ÖŠČÜŅŗpHµÄ¼ĘĖć£¬Ö»ÓŠĆ÷Č·ŅõŃō¼«ÉĻĪö³öµÄĪļÖŹ²ÅÄÜÕżČ·½ā“š£¬ĪŖŅדķµć£®


 53ĖęĢĆ²āĻµĮŠ“š°ø
53ĖęĢĆ²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šŹōŠŌĒæČõ£ŗNa£¾Mg£¾Al | B£® | ČČĪČ¶ØŠŌ£ŗHCl£¾H2 S£¾PH3 | ||
| C£® | ĖįŠŌĒæČõ£ŗHClO4£¾H2 SO4£¾H3PO4 | D£® | ČŪµć£ŗNa£¾SiO2£¾CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe3+”¢Na+”¢SCN-”¢Cl- | B£® | Na+”¢H+”¢NO3-”¢SO42- | ||
| C£® | Na+”¢OH-”¢H+”¢NO3- | D£® | Fe2+”¢NH4+”¢Cl-”¢OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ü¢Ż | B£® | ¢Ł¢Ż¢Ž | C£® | ¢Ł¢Ū¢Ü¢Ž | D£® | ¢Ś¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŹµŃ銔×éĪŖĢ½¾æSO2µÄĘư׊ŌŗĶ»¹ŌŠŌ£¬Éč¼ĘĮĖŅŌĻĀŹµŃ飮
ŹµŃ銔×éĪŖĢ½¾æSO2µÄĘư׊ŌŗĶ»¹ŌŠŌ£¬Éč¼ĘĮĖŅŌĻĀŹµŃ飮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
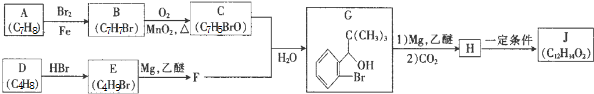
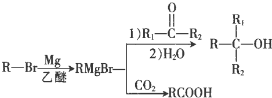
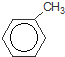 +Br2$\stackrel{Ģś·Ū}{”ś}$
+Br2$\stackrel{Ģś·Ū}{”ś}$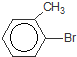 +HBr£®£¬Ęä·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£»
+HBr£®£¬Ęä·“Ó¦ĄąŠĶĪŖČ”“ś·“Ó¦£»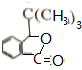 £¬ÓÉDÉś³ÉEµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖCH2=C£ØCH3£©2+HBr”ś£ØCH3£©3CBr£»
£¬ÓÉDÉś³ÉEµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖCH2=C£ØCH3£©2+HBr”ś£ØCH3£©3CBr£»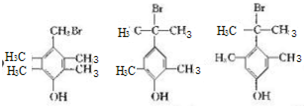 £ØĘäÖŠŅ»ÖÖ£©£ØŠ“³öŅ»ÖÖ¼“æÉ£©£®
£ØĘäÖŠŅ»ÖÖ£©£ØŠ“³öŅ»ÖÖ¼“æÉ£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀóŃæĢĒĖ®½āµÄ²śĪļÖ»ÓŠĘĻĢŃĢĒ | |
| B£® | ±½·ÓæÉÓĆÓŚŗĻ³Éøß·Ö×Ó»ÆŗĻĪļ | |
| C£® | ÓĶÖ¬Ė®½āæÉŅŌÖĘČ”øß¼¶Ö¬·¾Ėį | |
| D£® | ¼¦µ°ĒåÓö“×ĖįĒ¦ŗó²śÉśµÄ³ĮµķÄÜÖŲŠĀČÜÓŚĖ® |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com