
| A. | 18g重水含有10NA个电子 | |
| B. | 室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数约为3NA | |
| C. | 常温下0.05mol•L-1Fe2(SO4 ) 3溶液中含Fe 3+数目小于0.1NA | |
| D. | 用石墨作电极电解饱和食盐水时,若阴极得到2NA个电子,则阳极产生22.4L气体 |
分析 A、重水的摩尔质量为20g/mol;
B、乙烯和丙烯的最简式均为CH2;
C、溶液体积不明确;
D、气体所处的状态不明确.
解答 解:A、重水的摩尔质量为20g/mol,故18g重水的物质的量为0.9mol,而1mol重水中含10mol电子,0.9mol重水中含9mol电子即9NA个,故A错误;
B、乙烯和丙烯的最简式均为CH2,故42g混合物中含有的CH2的物质的量为n=$\frac{42g}{14g/mol}$=3mol,则含3mol碳原子即3NA个,故B正确;
C、溶液体积不明确,故溶液中的铁离子的个数无法计算,故C错误;
D、气体所处的状态不明确,故当阴极得到2NA个电子时,阳极失去2NA个电子,产生1mol氯气,但体积不一定为22.4L,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用胶头滴管取少量液体试剂 | B. | 用纸槽向试管底部加入粉未状药品 | ||
| C. | 用燃着的酒精灯点燃另一盞酒精灯 | D. | 用排水法收集难溶于水的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液和稀盐酸 | B. | NaHCO3溶液和稀盐酸 | ||
| C. | AlCl3溶液和NH3•H20溶液 | D. | 澄清石灰水和NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
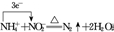 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | N2 | Cl2 | Br2 | I2 | O2 |
| 键能 (kJ•mol-1) | 945 | 243 | 193 | 151 | 498 |
| 键长(nm) | 0.110 | 0.199 | 0.228 | 0.266 | 0.121 |
| A. | N2>Cl2>Br2>O2>I2 | B. | O2>N2>I2>Br2>Cl2 | ||
| C. | I2>Br2>Cl2>O2>N2 | D. | N2>O2>Cl2>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 | |
| B. | 实验室制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 | |
| C. | 单质硅是生产光纤制品的基本原料 | |
| D. | 水玻璃可用于生产黏合剂和防火剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com