
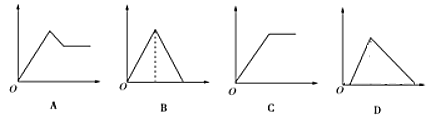
【题目】如图图象中,纵坐标为沉淀物的物质的量,横坐标为向溶液中加入反应物的物质的量,则相应的图像序号与(1)—(4)对应的是
溶液 | 加入物质 | 对应的图像 |
(1)饱和石灰水 | 通过量CO2气体 | ____ |
(2)氯化铝溶液 | 加入过量氨水 | ____ |
(3)MgCl2、AlCl3的混合液 | 逐滴加入NaOH溶液至过量 | ____ |
(4)含少量NaOH的NaAlO2溶液 | 逐滴加入稀盐酸 | ____ |
【答案】B C A D
【解析】
(1)饱和石灰水中通入过量CO2,发生反应:Ca(OH)2+CO2=CaCO3↓+H2O、CaCO3+CO2+H2O=Ca(HCO3)2,对应图象为B。答案为B。
(2)氯化铝溶液中加入过量氨水,发生反应:AlCl3+3NH3·H2O =Al(OH)3↓+3NH4Cl,对应图象为C。答案为C。
(3) MgCl2、AlCl3的混合液逐滴加入NaOH溶液至过量,发生反应:MgCl2+2NaOH=Mg(OH)2↓+2NaCl、
AlCl3+3NaOH=Al(OH)3↓+2NaCl、Al(OH)3+NaOH=NaAlO2+2H2O,起初生成沉淀,后来沉淀部分溶解,对应图象为A。答案为A。
(4)含少量NaOH的NaAlO2溶液逐滴加入稀盐酸,发生反应:NaOH+HCl=NaCl+H2O、
NaAlO2+HCl+H2O= Al(OH)3↓+NaCl、Al(OH)3+3HCl=AlCl3+3H2O,对应图象为D。答案为D。


科目:高中化学 来源: 题型:
【题目】测定硫酸铜晶体(CuSO4·xH2O)结晶水含量的实验流程如下:
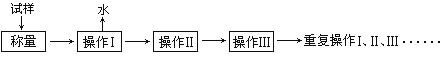
请回答:
(1)以下是实验中可能用到的几种仪器,请在图下方横线上写出仪器名称。
|
|
|
|
a. 电子天平 | b. ___________ | c. ____________ | d. 酒精喷灯 |
①“操作I”是灼烧硫酸铜晶体,将用到上述________(填序号)仪器;
②“操作Ⅱ”是____________,必须在________(填序号)中进行,否则将造成实验测定结果_____________(填“偏高”、“偏低”或“正确”)。
(2) “重复操作Ⅰ、Ⅱ、Ⅲ”,称为恒重操作。判断达到恒重的依据是____________________________________________;进行恒重操作的目的是____________________________________________。
(3)某学生实验后得到下表数据:
加热前质量 | 加热后质量 | |
m1(容器) | m2(容器+晶体) | m3(容器+无水硫酸铜) |
5.4 g | 7.9 g | 6.9 g |
① 由此该学生计算得出该硫酸铜晶体中结晶水x的值为________________(精确到0.1)。
② 指出该同学实验操作或数据处理中存在的主要问题____________(至少写2点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气因含有少量 H2S 等气体开采应用受限。T.F 菌在酸性溶液中可实现天然气的催化脱硫,其原理如下图所示。下列说法不正确的是( )
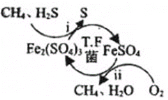
A.脱硫过程 O2 间接氧化 H2S
B.该脱硫过程需要不断添加 Fe2(SO4)3 溶液
C.亚铁是血红蛋白重要组成成分,FeSO4 可用于治疗缺铁性贫血
D.《华阳国志》记载“取井火煮之,一斛水得五斗盐”,我国古代已利用天然气煮盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的溶液是化学实验室的基本实验操作之一。请回答下列问题:
(1)配制0.5mol/L的硫酸溶液450mL,需用量筒量取质量分数98%、密度1.84g/cm3的浓硫酸的体积为___mL,如果实验室有15mL、20mL、50mL量筒,应最好选用___mL量筒。
(2)配制上述溶液,除用到量筒、烧杯、玻璃棒外,还需要的两种玻璃仪器是___。
(3)关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是__(填字母)。
A.①②③④ B.②③ C.①②④ D.②③④
(4)配制时,其正确的操作顺序是___(用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有水的烧杯中加入浓硫酸稀释
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(5)下面操作造成所配稀硫酸溶液浓度偏高的是__(填序号)。
A.浓硫酸稀释后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量浓硫酸后洗涤量筒并将洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①稀硫酸 ②氧化铝固体 ③氨水 ④二氧化碳 ⑤FeCl3固体 ⑥稀NaOH溶液,按要求填空:
(1)上述物质中属于电解质的物质序号为______ ;
(2)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______;
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______;试用离子方程式说明:_______________、______________;
(4)能导电的物质序号为_______________;
(5)实验室用⑤制备胶体的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)质量比为14 :15的N2和NO混合,则混合气体中氮原子和氧原子的个数比为________
(2)同温同压下,质量相同的五种气体:①CO2 ②H2 ③O2 ④CH4 ⑤SO2所占的体积由大到小的顺序是(填序号,下同)_________________;
(3)已知19g某二价金属的氯化物RCl2中含有0.4mol的Cl-离子,则R的相对原子质量为______________________ ;
(4)在Al2(SO4)3和MgSO4组成的混合物中,Al3+与Mg2+的物质的量之比为2∶1,则在含有2mol SO42-的混合物中,MgSO4的质量是________________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从元素化合价变化的角度分析,下列反应中,画线的物质发生氧化反应的是
A. SO2 + 2NaOH = Na2SO3 + H2O B. 2CuO + C![]() 2Cu + CO2↑
2Cu + CO2↑
C. 2FeCl3 + Fe = 3FeCl2 D. Zn+2HCl = ZnCl2+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
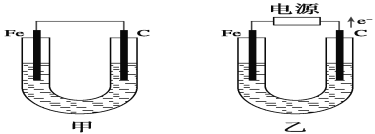
(1)若两池中电解质溶液均为CuSO4溶液,则反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒。
②乙池中阳极的电极反应式是__________________________________。
(2)若两池中电解质溶液均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式_______________________________。
②甲池中碳极上电极反应式是____________________________,乙池碳极上电极反应属于______________(填“氧化反应”或“还原反应”)。
③将湿润的KI淀粉试纸放在乙池碳极附近,发现试纸变蓝,反应的化学方程式为________________________________________。
④若乙池转移0.02 mol e-后停止实验,池中电解质溶液体积是200 mL,则溶液混合均匀后的c(OH—)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘酸钙[Ca(IO3)2]广泛用于食品工业、口腔洗涤,防腐等领域,某化学兴趣小组在实验室利用碘在酸性条件下被氯酸钾氧化成碘酸氢钾(KIO3·HIO3),溶液经氢氧化钾中和后,与氯化钙发生复分解反应制备碘酸钙,其制备步骤及装置(水浴加热装置略去)如图: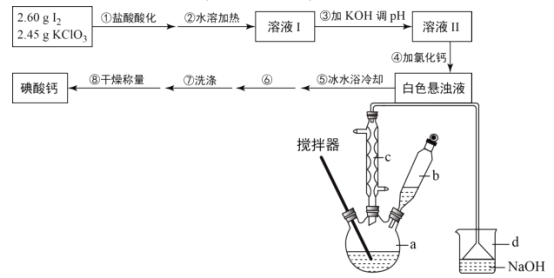
物质的摩尔质量如下表:
物质 | I2 | KClO3 | Ca(IO3)2 |
摩尔质量/g·mol-1 | 354 | 122.5 | 390 |
请回答下列问题:
(1)加入b中盐酸后,碘在酸性条件下被氯酸钾氧化成碘酸氢钾(KIO3·HIO3),反应中有黄绿色的气体生成,该反应的化学方程式为___。
(2)步骤②与“直接加热”相比,“水浴加热”的优点为___。
(3)步骤④加入氯化钙后,得到白色悬浊液,说明KIO3的溶解度___(填“大于”“小于”或“等于”)Ca(IO3)2。
(4)步骤⑤冰水浴冷却的目的为___。
(5)步骤⑥的操作名称为___。
(6)步骤⑦洗涤后检验沉淀是否洗涤干净的方法为___。
(7)最终得到2..60g碘酸钙产品,则产率为___ %(保留2小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com