
【题目】A、B、C、D是四种短周期元素,E是过渡元素.A、B、C同周期,C、D同主族,A的原子结构示意图为:![]() ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E元素的正三价离子的3d亚层为半充满.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E元素的正三价离子的3d亚层为半充满.回答下列问题:
(1)写出下列元素的名称:A________, B________, C________,D________。
(2)用元素符号表示D所在周期第一电离能最大的元素是__________,电负性最大的元素是__________。
(3)D的氢化物比C的氢化物的沸点__________(填“高“或“低“),原因__________。
(4)E元素的正三价离子的电子排布式为________________________。E元素在周期表中的位置是_________。
(5)用电子式表示B的硫化物的形成过程:_____________________________________。
(6)写出A的最高价氧化物与B的最高价氧化物的水化物反应的离子方程式________。
【答案】 硅 钠 磷 氮 Ne F 高 因为NH3分子间形成氢键 [Ar]3d5 第四周期,第Ⅷ族 ![]() SiO2+2OH﹣=SiO32﹣+H2O
SiO2+2OH﹣=SiO32﹣+H2O
【解析】(1)根据A的原子结构示意图知道x=2,所以A为硅,B与A同周期且电离能最小,所以B为钠,C为第三周期元素且最外层有三个成单电子,所以C的价电子排布式为3p3,所以C为磷,D与磷同主族且为短周期元素,所以D为氮, E元素的正三价离子的3d亚层为半充满,所以E的三价离子的价电子排布式为3d5,则其原子的价电子排布式为3d64s2,所以E为铁。
(2)D为N元素属于第二周期,第二周期所有的元素中,稀有气体元素Ne原子最外层为8个电子的稳定结构,故其电离能最大,F元素的非金属最强,吸引电子的能力也越强,故电负性最大的是F 。
(3)D的氢化物为NH3,C的氢化物为PH3,NH3分子间存在氢键,所以NH3的沸点高于PH3,答案为:高、因为NH3分子间形成氢键。
(4)Fe原子的价电子排布式为3d64s2,失去3个电子后变成Fe3+,其电子排布式为[Ar]3d5,Fe的电子排布式为1s22s22p63s23p63d64s2,所以Fe在周期表中的位置为第四周期第Ⅷ族。
(5)Na2S为离子键形成的离子化合物,构成的粒子为阴阳离子,用电子式表示其形成过程时,左边为原子的电子式,右边为离子的电子式,具体表示如下:![]()
(6)二氧化硅与氢氧化钠溶液反应的离子方程式为:SiO2+2OH﹣=SiO32﹣+H2O


科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.传统的无机非金属材料具有抗腐蚀性、耐高温等许多优点,但也有质脆、经不起热冲击的缺点
B.新型无机非金属材料继承了传统非金属材料的优点,但不能耐高温
C.有些新型无机非金属材料可以做绝缘体,但都不能做半导体
D.新型无机非金属材料都能透过可见光
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是恒温下某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( ) 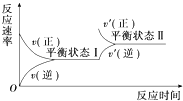
A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡状态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡状态Ⅱ
C.该反应达到平衡状态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡状态Ⅱ
D.同一种反应物在平衡状态Ⅰ和平衡状态Ⅱ时浓度不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2O32-+O2+aOH-=Y+S4O62-+2H2O,下列说法中,不正确的是
A.a = 4B.Y的化学式为Fe2O3
C.S2O32-是还原剂D.每有1molO2参加反应,转移的电子总数为4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为HO-CH2CH=CHCH2-COOH,该有机物不可能发生的化学反应是( )
A. 水解 B. 酯化 C. 加成 D. 氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列一步转化中,一定要加入氧化剂才能实现的是( )
A. SiO2―→Na2SiO3 B. Na2O2―→NaOH
C. N2―→NH3 D. NH3―→NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下反应:X(g)+Y(g) ![]() Z(g)+W(s), △H>0下列叙述正确的是( )
Z(g)+W(s), △H>0下列叙述正确的是( )
A. 加入少量W,逆反应速度增大 B. 当容器中气体压强不变时,反应达到平衡
C. 升高温度,平衡逆向移动 D. 平衡后加入X,上述反应的△H增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com