


 .
. )有多种属于酯类的同分异构体,其中能与FeCl3溶液发生显色反应,且苯环上的一硝基取代物只有两种同分异构体的结构简式有
)有多种属于酯类的同分异构体,其中能与FeCl3溶液发生显色反应,且苯环上的一硝基取代物只有两种同分异构体的结构简式有 (其中两种)(任写两种即可).
(其中两种)(任写两种即可). 分析 苯和氯气发生取代反应生成氯苯,氯苯和氢氧化钠的水溶液发生取代反应生成苯酚,苯酚和氢氧化钠反应生成苯酚钠;苯酚钠和乙反应生成苯氧乙酸和丙,根据题给信息知,乙是2-氯乙酸,甲和氯气发生取代反应生成2-氯乙酸,则甲是乙酸;1mol丙完全燃烧可产生3mol CO2和3mol H2O,则丙分子中含有3个碳原子6个氢原子,且丙的相对分子质量为58,则丙的分子式为C3H6O,且丙分子中不含甲基,为链状结构,则丙是丙烯醇,苯氧乙酸和丙烯醇发生酯化反应生成苯氧乙酸丙烯酯,则丁是苯氧乙酸丙烯酯.
解答 解:苯和氯气发生取代反应生成氯苯,氯苯和氢氧化钠的水溶液发生取代反应生成苯酚,苯酚和氢氧化钠反应生成苯酚钠;苯酚钠和乙反应生成苯氧乙酸和丙,根据题给信息知,乙是2-氯乙酸,甲和氯气发生取代反应生成2-氯乙酸,则甲是乙酸;1mol丙完全燃烧可产生3mol CO2和3mol H2O,则丙分子中含有3个碳原子6个氢原子,且丙的相对分子质量为58,则丙的分子式为C3H6O,且丙分子中不含甲基,为链状结构,则丙是丙烯醇,苯氧乙酸和丙烯醇发生酯化反应生成苯氧乙酸丙烯酯,则丁是苯氧乙酸丙烯酯.
(1)苯酚和氢氧化钠溶液反应生成苯酚钠,根据原子守恒知,试剂X可能是氢氧化钠或碳酸钠,甲是乙酸,乙酸和氯气发生取代反应生成2-氯乙酸,所以反应Ⅳ的反应类型是取代反应,
故答案为:氢氧化钠或碳酸钠,取代反应;
(2)通过以上分析知,丙的分子式为C3H6O,其所含官能团的名称为碳碳双键和醇羟基,
故答案为:C3H6O,碳碳双键和醇羟基;
(3)乙是2-氯乙酸,则乙的结构简式是CH2ClCOOH,苯氧乙酸和丙烯醇发生酯化反应生成苯氧乙酸丙烯酯,所以反应Ⅵ的化学方程式是 ,
,
故答案为:CH2ClCOOH, ;
;
(4)苯氧乙酸有多种属于酯类的同分异构体,其中能与FeCl3溶液发生显色反应,说明其同分异构体中含有酚羟基,且苯环上的一硝基取代物只有两种,则符合条件的苯氧乙酸的同分异构体结构简式有: ,
,
故答案为: (其中两种).
(其中两种).
点评 本题考查了有机物的推断,以苯酚钠和苯氧乙酸为突破口采用正逆相结合的方法推断其它物质,明确有机物的官能团及其性质是解本题关键,难点是同分异构体的判断,注意不仅有官能团异构还有位置异构,难度中等.


 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:选择题
| A. | ③>①>②>④ | B. | ④>③>①>② | C. | ③>①=④>② | D. | ①=③=④>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 混合物 | X | Y |
| ① | C3H6、C2H4 | m | 15m/7 |
| ② | HCHO、HCOOH | m | 15m/23 |
| ③ | CH3OH、CH3COOH | m | m |
| ④ | HCOOH、CH3COOCH3 | m | m |
| A. | ①② | B. | ③② | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 组成上相差一个或若干个CH2 原子团,且符合同一通式的有机物之间互称为同系物 | |
| B. | 苯分子结构中不存在碳碳双键,因此苯不能发生加成反应 | |
| C. | 相同条件下,正丁烷、正戊烷、正己烷的沸点依次减小 | |
| D. | 皮肤上不小心沾上苯酚的浓溶液可用酒精清洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量铁粉加入稀硝酸中:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| B. | H2SO4溶液与Ba(OH)2溶液反应:Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O | |
| C. | NaHCO3溶液和过量Ba(OH)2溶液共热:HCO3-+OH-+Ba2+═BaCO3↓+H2O | |
| D. | 苯酚溶液中滴加Na2CO3溶液: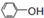 +CO32-→HCO3-+ +CO32-→HCO3-+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
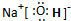 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH${\;}_{4}^{+}$ | SO${\;}_{4}^{2-}$ | NO3 | Cl- |
| 浓度/mol•L-l | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
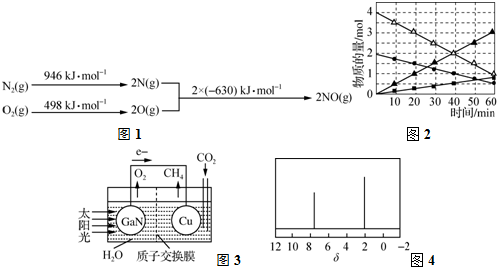
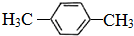 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com